Аменорея при миоме матки
 | МИФ 1: Миома матки — это почти рак или «предраковое» состояниеНа самом деле. Миома матки никак не связана с онкологическими заболеваниями, не вызывает их и даже не является предрасполагающим фактором. |
Единственная злокачественная опухоль из гладкомышечных клеток матки (лейомиосаркома) — это одна из наиболее редко встречающихся опухолей мягких тканей. Она может возникнуть в матке, но как самостоятельное заболевание, а не в результате злокачественного превращения миомы матки. Таким образом, рассуждения врача на тему о возможности развития рака из миомы безосновательны и не могут быть показанием к выполнению радикальной операции. Это очень распространенное заблуждение, помогающее убеждать пациенток с миомой согласиться на удаление матки.
Если узел быстро растет, нет причин сразу впадать в панику. Это не говорит о том, что миома «превратилась в рак», и результаты многочисленных научных исследований — тому подтверждение. Как правило, быстрый рост обусловлен вторичными (дегенеративными) изменениями в узле и его отеком.
Поэтому, если доктор предлагает радикальную операцию, аргументируя это тем, что миома может оказаться злокачественной опухолью или с высокой вероятностью трансформируется в рак — вполне возможно, что стоит сменить доктора и получить еще одну независимую консультацию.
Важно отметить, что речь идет только о злокачественной опухоли мышцы матки. Миома — не рак, но это не исключает возможности развития злокачественного новообразования в других отделах матки (слизистой оболочки эндометрия) или шейки матки (хотя меры профилактики и раннего выявления известны, совсем несложны и доступны). Но эти процессы не связаны с наличием миомы, и диагноз «миома матки» нисколько не повышает риск развития этих заболеваний.
 | МИФ 2: Миома — от гормонов, нужно первым делом сдать анализы на гормоныНа самом деле. При обследовании пациентки с миомой матки анализы на гормоны, как правило, не нужны. |
Нередко при постановке диагноза «миома матки» врач назначает обследование «на гормоны», видимо, предполагая, что эти данные позволят ему пролить свет на причины возникновения миомы и помогут выбрать правильное лечение.
На самом деле необходимости в подобных анализах нет.
- Миома — это локальная патология мышечного слоя стенки матки, и каждый узел растет в результате повреждения одной клетки.
- Уровень гормонов никак не влияет на возникновение этого узла и не определяет развитие заболевания.
- Миома матки выявляется у женщин с нормальным менструальным циклом, женщины легко беременеют и рожают с миомой матки.
- Выбор метода лечения миомы никак не связан с уровнем половых гормонов.
Это лишнее обследование, которое вам проходить не надо, и если доктор предлагает его и указывает на его значение в диагностике и лечении — стоит усомниться в том, что доктор понимает природу этого заболевания и сможет рекомендовать вам правильный метод лечения.
Влияют ли гормональные препараты на рост миомы матки? Узнайте о применении гормональных препаратов в лечении миомы матки!
 | МИФ 3: При диагнозе «миома матки» первым делом нужно проводить выскабливание (чистку)На самом деле. Выскабливание полости матки не нужно проводить всем подряд пациенткам с миомой матки. |
Выскабливание полости матки проводится по строгим показаниям, к которым относятся:
- выявленные при УЗИ полипы,
- гиперплазия эндометрия,
- маточные кровотечения неясного происхождения,
- жалобы на межменструальные кровянистые выделения.
Во всех остальных случаях, когда у пациентки умеренные не длительные менструации, а при УЗИ хорошо просматривается эндометрий, и в нем нет патологических изменений, достаточно провести аспирационную биопсию (пайпель-биопсию) эндометрия. Это безболезненная амбулаторная процедура, которая проводится без наркоза.
В результате выскабливания, как и при аспирационной биопсии, можно получить информацию о состоянии слизистой оболочки матки (эндометрия), но эти диагностические методы не дают никакой информации о состоянии миоматозных узлов, как это нередко объясняется пациенткам. Это исследование необходимо только для исключения патологии эндометрия, которая бы могла помешать органосохраняющему лечению миомы матки.
 | МИФ 4: Миому всегда нужно активно лечить!На самом деле. Миома матки, не сопровождающаяся симптомами, у женщины, не планирующей беременность, не требует лечения. |
Не все миоматозные узлы прогрессивно растут во время репродуктивного периода женщины. Часть узлов может вырасти до определенного размера и затем остановиться в росте или медленно прогрессировать со скоростью, скажем, 5 мм в год. Если узлы не деформируют полость матки, нет никаких клинических проявлений (то есть они не влияют на качество жизни женщины) — лечение в таком случае не требуется, достаточно динамического наблюдения.
Надо отметить, что пациентки не всегда могут сформулировать на приеме у врача, какие симптомы их беспокоят (обильные менструации, ощущение давления на мочевой пузырь, увеличение живота), поэтому в любом случае надо проходить осмотр у гинеколога, делать УЗИ и оценивать уровень гемоглобина. К примеру, падение гемоглобина может указывать на неправильную оценку обильности менструаций, а увеличение талии или рост живота может быть принято за набор веса, а не рост миоматозных узлов. Но соглашаться на операцию, если симптомы полностью отустствуют, не стоит.
 | МИФ 5: Даже маленькую миому нужно удалить — «для профилактики»На самом деле. Невозможно прогнозировать динамику роста узлов миомы матки и предсказывать прогноз развития заболевания. В связи с этим профилактические хирургические вмешательства в отношении миомы матки недопустимы, как и удаление матки, проводимое только в связи с отсутствием желания пациентки в дальнейшем иметь детей. |
При выборе метода лечения миомы матки врач не может оперировать своими собственными предположениями о том, как будет развиваться заболевание, и к каким последствиям может привести бездействие пациентки. Миома матки — образование с весьма непредсказуемым характером роста, поэтому оценивать его нужно в динамике, учитывая жалобы, возраст пациентки и ее планы на беременность. Важно помнить, что миома матки — заболевание, которое закончится в менопаузе, то есть у миомы есть свой логический конец.
Отношение к матке как к органу только для вынашивания детей также недопустимо, так как матка вовлечена в целый ряд важнейших процессов в организме, обеспечивает полноценную половую жизнь и формирование оргазма. Удаление матки может существенно отразиться на здоровье (повышается риск сердечно-сосудистых заболеваний и метаболических нарушений), что подтверждают сотни убедительных зарубежных исследований. Печально, что некоторые гинекологи предпочитают забыть об этих данных, чтобы уговорить пациентов на удаление матки.
 | МИФ 6: Удалить матку — это так просто и здорово! И никаких проблем потом!На самом деле. Удаление матки — это не «простая и безопасная операция без каких-либо последствий для организма» и не может рассматриваться, как основной метод лечения миомы матки у женщин, не планирующих беременность |
Любое хирургическое вмешательство, даже очень простое может иметь самые серьезные последствия, включая летальный исход. Прогнозировать развитие редких, но возможных осложнений, весьма затруднительно. Поэтому у опытных грамотных хирургов существует фраза: «Лучшая операция та, без которой удалось обойтись». Хирургическое вмешательство всегда нужно проводить по строгим показаниям и преимущественно в тех случаях, когда без него невозможно обойтись, нет никакой альтернативы, и если его не выполнить, возможна угроза для жизни пациента, либо для ее качества. Если есть хотя бы какая-то адекватная возможность избежать хирургической операции — надо постараться избежать операции.

В подавляющем большинстве случаев пациенткам с миомой матку удаляют, не предложив никакой альтернативы, представив это вмешательство как простое и безопасное, не имеющее никаких последствий для организма. Нередко на подобное вмешательство попадают бессимптомные пациентки, запуганные ужасными последствиями своего заболевания.
Последствия удаления матки с придатками или без достаточно хорошо изучены. Доказано, что у таких пациенток значительно чаще развиваются сердечно-сосудистые заболевания, появляются проблемы с весом, эндокринные нарушения и повышается вероятность развития трех видов злокачественных опухолей.
Отдельной группой стоят заболевания нервной системы, расстройства настроения и мотивации. Все эти неприятные явления, как правило, развиваются не сразу после операции, а в течение последующих лет, поэтому пациенты часто не связывают их с перенесенным хирургическим вмешательством и начинают лечение у других специалистов. Аналогично, гинекологи перестают видеть этих женщин, и у них создается ложное впечатление, что всё в порядке.
Удаление матки не должно приниматься, как единственно возможный и простой метод лечения миомы. Удаление матки — это последний шаг в списке всех возможных методов лечения, к которому надо прибегать только в крайнем случае. Бегите от доктора, который говорит вам подобные вещи: «Не бойтесь, это простая операция, такие операции выполняются сотнями тысяч, осложнений практически нет, вы быстро вернетесь к обычной жизни, так как это будет лапароскопическая операция, никаких последствий, вы мне только спасибо скажете, зачем вам с этим мешком с узлами ходить, ведь рожать вы больше не собираетесь…»
 | МИФ 7: Раз есть миома — забудь о бане и загаре!На самом деле. Пациенткам с миомой матки не противопоказан загар, бани, сауны и массаж, так как нет научных доказательств влияния этих факторов на рост и развитие узлов миомы. |
Нам не удалось найти ни одного достоверного научного исследования, которое бы показало связь между перечисленным физическими воздействиями и ростом миоматозных узлов. Все рассуждения на этот счет имеют исключительно умозрительный характер. Это совсем не означает, что узнав об этом, надо без разумных ограничений целый день загорать под палящим солнцем или часами просиживать в сауне. Просто при миоме матки вам не стоит вносить существенные изменения в свой привычный уклад жизни и ограничивать себя, постарайтесь во всём соблюдать умеренность и избегайте злоупотреблений.
 | МИФ 8: Раз есть миома, то родить уже не удастся!На самом деле. Миома матки практически никогда не бывает причиной бесплодия, но может быть причиной невынашивания беременности. Не во всех случаях необходимо удаление миоматозных узлов перед беременностью |
Влиять на течение беременности и мешать её развитию могут узлы, которые растут в полость матки или существенно деформируют её. Не все узлы могут потенциально помешать протеканию беременности, и совсем не обязательно перед беременностью удалять из матки все миоматозные узлы, включая маленькие и растущие снаружи матки. Важно правильно оценить значение этих узлов для беременности, и принять правильное решение: что будет более рискованным для женщины — беременности с такими узлами или беременности с рубцами на матке после удаления этих узлов.
Сейчас все больше женщин выходят на беременность с миомой. Грамотные репродуктологи проводят ЭКО пациенткам с миоматозными узлами в матке с хорошим результатом. Другими словами, страх перед миомой матки в аспекте беременности и родов прошел. В настоящий момент больше неприятностей могут представлять рубцы, после удаления узлов из матки, не всегда хорошо ушитых, и вследствие этого повышающих риск разрыва матки, врастания плаценты и других грозных акушерских осложнений.
 | МИФ 9: Размеры миомы на УЗИ определяются с высокой точностью! Если вчера было 25 мм, а сегодня 28 мм, то узел вырос!На самом деле: Оценка динамики роста миоматозных узлов по УЗИ часто сопровождается погрешностями измерения. Наиболее объективный метод оценки миоматозных узлов — МРТ. |
Нередко бессимптомной пациентке с миомой матки сообщают, что за последнее время её узел (или узлы) существенно выросли, и это повод удалить матку, так как заболевание прогрессирует и «мало ли чего еще может быть…».
Надо помнить, что миоматозный узел по форме не шар, не овал и даже не квадрат. Миома по форме более всего напоминает картошку (нашу отечественную, а не импортную идеальной формы и симметрии). То есть в двухмерной плоскости её можно измерить по-разному, и разница между размерами может быть существенной.
Для объективной оценки роста узлов нужно не только фиксировать 2-3 замера узла, но и делать соответствующие фотографии, чтобы потом увидеть, в каких плоскостях производились измерения. Или использовать объективный метод диагностики — МРТ. Всё это означает, что если у вас нет никаких жалоб, и на очередном визите к гинекологу вас испугали быстрым ростом узлов — паниковать не надо. Во-первых, как уже отмечалось выше, быстрый рост совершенно не говорит о том, что это онкологическое заболевание, а во-вторых — это может быть элементарная погрешность в измерении узла. В таких случаях надо зафиксировать эти размеры, сделать фото или МРТ и повторить замеры через 3-4 месяца. Это оптимальный срок чтобы увидеть тенденцию к росту узлов и не запустить заболевание.
 | МИФ 10: Можно вылечить миому биодобавками, травами и прочими «чудодейственными» методамиНа самом деле. «Индинол», «Эпигалат», биорезонансная терапия, боровая матка, травы, пиявки не являются методами лечения миомы матки |
«Индинол», «Эпигалат» — это не лекарственные препараты, то есть эти вещества по определению не могут оказывать лечебного воздействия на организм. Это биологически активные добавки к пище. Единственное, что они могут делать, это восполнить недостаток витаминов или микроэлементов в организме. Время и деньги, потраченные на «лечение» этими препаратами, будут выброшены на ветер. Это же касается и боровой матки и какой-то там щетки, и прочим широко предлагаемым методам лечения миомы матки.
Миоматозные узлы состоят из мышечных и фиброзных волокон — как очень сухое и жилистое мясо. Они расположены в стенке матки (это мышечная ткань), то есть по структуре узлы как обычный кусок мяса. Невозможно с помощью различных таблеток, отваров или пиявок «из одного куска мяса удалить другой кусок мяса». Его можно или вырезать, или избирательно лишить кровоснабжения, чтобы он погиб и «засох». Этот пример приведен для того, чтобы вы правильно понимали, чем на самом деле является ваше заболевание и реалистично смотрели на эффективность того или иного метода лечения.
 | МИФ 11: Лечение миомы начинают с «Дюфастона». Авось поможет!На самом деле. «Дюфастон» противопоказан пациенткам с миомой матки в качестве основного метода лечения этого заболевания. |
Этот парадокс все никак не уйдет в историю. Пациенток с миомой матки продолжают лечить дюфастоном, в то время как выходит уже второе поколение препаратов для уменьшения узлов миомы матки с полностью противоположным дюфастону эффектом воздействия на ткань узлов.
Дюфастон — это полный аналог натурального гормона прогестерона. Этот гормон и есть основной фактор, стимулирующий рост миоматозных узлов. Другими словами, дюфастон только стимулирует рост узлов, а не уменьшает их. Самый последний появившийся на рынке препарат для лечения миомы матки Эсмия избирательно блокирует рецепторы прогестерона, не давая ему реализовывать свой эффект на клетки, что приводит к прекращению роста узлов и их уменьшению, но этот эффект обратимый, так как препарат нельзя принимать долго. Таким образом, дюфастон выращивает миоматозные узлы, а не лечит миому матки. И если доктор вам назначил этот препарат в качестве лечения миомы матки (кроме одного случая: дюфастон может быть обоснованно назначен, чтобы вызвать менструации, и это допустимо) — меняйте доктора.
 | МИФ 12: Если есть миома — нужно вырезать миому!На самом деле. Хирургическое удаление миоматозных узлов у женщин, не планирующих беременность, совершенно лишено смысла. По крайней мере, с тех пор как существует альтернатива в виде эмболизации маточных артерий (ЭМА). |
В большинстве случаев миомэктомия (удаление узлов из матки) — это операция, направленная на временное восстановление анатомии матки, чтобы позволить женщине выносить и родить ребенка. Временный эффект миомэктомии связан с высокой частотой рецидивов роста узлов (10–15% в год!). Если женщина не планирует беременность, и у неё есть симптомная миома матки — в подавляющем большинстве случаев надо отдать предпочтение эмболизации маточных артерий. Почему? Дело в том, что ЭМА с эффективностью в 96–98% устраняет все симптомы миомы матки, то есть решает основную проблему женщины, влияющую на качество жизни.
Вероятность рецидива заболевания после ЭМА составляет менее 2% за весь период наблюдения. Причем, как правило, такой рецидив связан с восстановлением кровотока и легко устраняется дополнительной процедурой. Таким образом, благодаря ЭМА, пациентка решает проблему миомы матки раз и навсегда. И при этом ей не приходится подвергаться общему наркозу и полостной операции. Это в полной мере относится и к лапароскопическим операциям, частота осложнений при которых еще выше, чем при обычных (лапаротомных) операциях.
Очевидно, что сложная и относительно длительная операция под общим наркозом, сопровождающаяся кровопотерей, с целым списком из десятков возможных осложнений, а также приводящая к рецидивам — не самый оптимальный путь в решении проблемы обильных менструаций или чувства давления на мочевой пузырь, когда есть альтернатива в виде эмболизации маточных артерий.
Источник
Статья посвящена возможностям медикаментозного лечения миомы матки в период менопаузального перехода. Показано, что пролонгированное лечение мифепристоном
(Гинестрил) отличается эффективностью и высоким профилем безопасности.
Введение
Миома матки (ММ) является одним из наиболее распространенных гинекологических заболеваний, которое ассоциируется с высоким риском аномального маточного кровотечения, дисменореи, при этом на сегодняшний день не существует прогностических маркеров, позволяющих оценить степень ответа на лечение и риски рецидива или прогрессирующего течения заболевания [1], что в итоге ограничивает возможности персонифицированного выбора оперативной, лекарственной или комбинированной терапии [2].
Цель нашего исследования — оценить отдаленные исходы пролонгированного лечения мифепристоном у пациенток с ММ в пременопаузе.
Материал и методы Дизайн исследования
С 2012 г. по апрель 2014 г. проведено проспективное долгосрочное исследование влияния пролонгированного лечения мифепристоном на течение ММ у женщин в пременопаузе.
Критерии включения в исследование:
возраст 40 лет и старше в момент включения в исследование;
наличие симптомной ММ (наличие хронического аномального маточного кровотечения);
пременопаузальный период («-2 стадия» по STRAW 10);
размеры доминантного миоматозного узла (эхографически определяемый диаметр) 4,0–5,5 см;
отсутствие в анамнезе полостных, в т. ч. выполненных лапароскопическим доступом, гинекологических операций;
отсутствие в анамнезе применения гормональной терапии ММ;
категорический отказ от хирургического лечения;
отсутствие противопоказаний к назначению мифепристона;
желание пациентки участвовать в исследовании и наличие информированного письменного согласия.
Критерии исключения из исследования:
возраст пациентки моложе 40 лет и старше 48 лет в момент включения в исследование;
размеры доминантного миоматозного узла менее 4,0 см и более 5,5 см;
анемия тяжелой степени в момент включения в исследование (уровень гемоглобина менее 70 г/л);
применение гормональной терапии ММ в анамнезе;
сахарный диабет и другие нарушения углеводного обмена, некомпенсированное нарушение функции щитовидной железы и других желез внутренней секреции (гипофиз, надпочечники, паращитовидные железы), в т. ч. требующее назначения заместительной гормональной терапии;
психиатрические заболевания, алгоколизм, наркомания, злокачественные новообразования, лимфопролиферативные заболевания и гемобластозы в анамнезе;
индекс массы тела по Броку более 34,9 кг/м2 и менее 18,5кг/м2;
ВИЧ-инфекция, хронические вирусные гепатиты В
и/или C в анамнезе;
нежелание пациентки участвовать в исследовании или низкая комплаентность.
Этические правила и нормы
Исследование выполнено в соответствии с принципами Хельсинкской декларации Всемирной ассоциации «Этические принципы научных и медицинских исследований с участием человека», законодательством Российской Федерации (Федеральный закон от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», Федеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств») и Правилами клинической практики в Российской Федерации, утвержденными приказом Минздрава России от 19.06.2003 № 266, и другими нормативными актами, содержащими требования к проведению клинических исследований и наблюдательных программ в Российской Федерации. Протокол наблюдения за пациентками и программа обследования были одобрены локальным этическим комитетом.
Обследование пациенток перед включением в исследование
Всем пациенткам, соответствующим критериям включения (по данным анамнеза и ультразвукового исследования (УЗИ) трансвагинальным датчиком), до начала лечения, с целью выявления критериев исключения, выполнялось обследование: скрининговые клинические и эпидемиологические анализы; гормональное обследование на 2–5-й день менструального цикла (определение уровней фолликулостимулирующего гормона, эстрадиола, тиреотропного гормона, пролактина); определение уровней гликированного гемоглобина, железа в сыворотке крови, ферритина, опухоль-ассоциированных серологических маркеров (альфа-фетопротеин, раково-эмбриональный агент); маммография; УЗИ щитовидной железы, органов брюшной полости, почек и надпочечников; пайпель-биопсия эндометрия с последующим патоморфологическим исследованием, за исключением случаев, когда имелись результаты гистологического исследования эндометрия давностью до 1 года.
Для участия в дальнейшем наблюдении было отобрано 46 женщин в возрасте от 44 до 48 лет (средний возраст — 45,9±1,9 года) в момент включения в исследование, с одиночной или множественной ММ (табл. 1).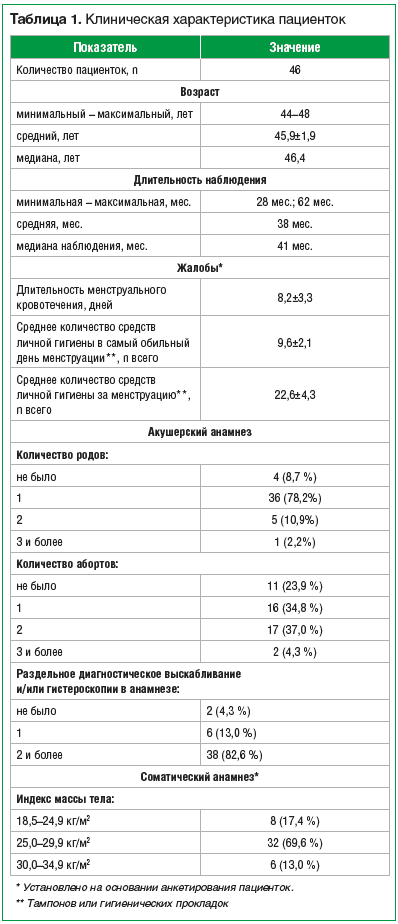
Режим приема мифепристона
Пациентки с ММ получали мифепристон по 50 мг через день (1 раз в 2 сут). Если пациентка по каким-либо причинам забывала принять таблетку, мифепристон принимался ежедневно до восстановления «календаря» приема препарата.
Наблюдение за пациентками
Все включенные в исследование пациентки наблюдались 1 раз в 3 мес. в течение всего периода лекарственного лечения ММ и в течение года после прекращения приема мифепристона. Далее наблюдение за течением ММ осуществлялось 1 раз в 6 мес. до наступления менопаузы. В ходе наблюдения методом трансвагинального УЗИ оценивались линейные размеры матки (количество и объем визуализированных миоматозных узлов, наибольший диаметр каждого узла) (табл. 2). В период лекарственного лечения (через 3, 6, 9 и 12 мес. от начала) у всех пациенток проводился забор венозной крови для клинического анализа крови и анализа сывороточного железа, ферритина. После окончания лечения всем пациенткам выполнялась пайпель-биопсия эндометрия с последующим гистологическим исследованием.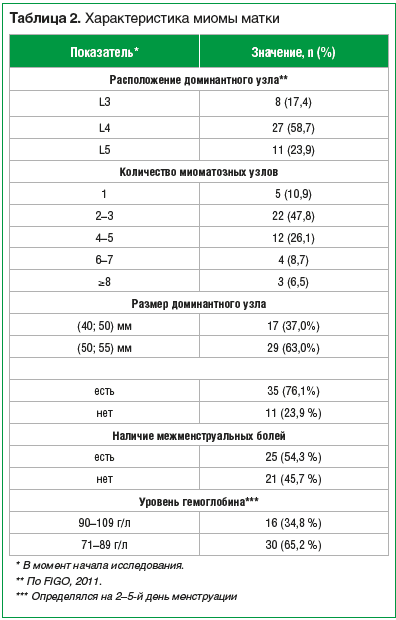
Статистический анализ результатов исследования
В проведенном клиническом исследовании не сравнивались разные режимы лечения, а оценивалась эффективность одного режима лекарственной терапии относительно исходных данных. При дальнейшем наблюдении (от окончания лечения до наступления менопаузы) никакие измеряемые показатели и статистические гипотезы предварительно не определялись. Описание количественных признаков, соответствующих нормальному распределению, представлено в виде среднего значения ± стандартное квадратичное отклонение; признаки, отличающиеся от нормального распределения — в виде медианы, качественные признаки — в виде долей (%) и абсолютных чисел. Метод определения достоверности сравниваемых признаков выбирался в зависимости от анализируемых данных. Результаты подвергали статистической обработке на персональном компьютере с помощью программ Excel, SPSS Statistics 22.0.
Результаты исследования
Первичные результаты исследования
Все включенные в исследование пациентки завершили исследование согласно дизайну. Данные четырехкратного эхографического исследования органов малого таза, лабораторных и инструментальных исследований, динамика жалоб пациенток представлены в таблице 3.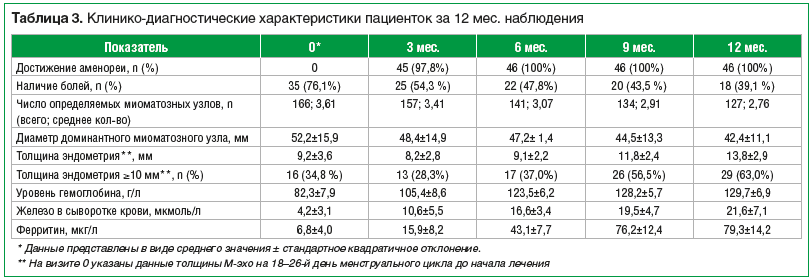
Несмотря на увеличение толщины М-эхо более 10 мм у 63,0% пациенток после 12 мес. лечения, по результатам патоморфологического исследования биоптата эндометрия во всех образцах данных за гиперпластические процессы или новообразования не получено.
Наблюдение за пациентками после окончания лекарственной терапии
После завершения лечения мифепристоном последующее наблюдение за пациентками проводилось до наступления менопаузы. Данные четырехкратного эхографического исследования представлены в таблице 4.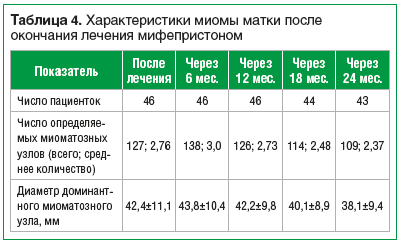
В целом за первые 36 мес. наблюдения суммарная частота рецидивов (увеличение одного или нескольких узлов на 20% и более) составила 21,7% (рис. 1). В 9 из 10 случаев прогрессирование в дальнейшем сменялось стабилизацией (6 случаев) и/или регрессией (3 случая), одной пациентке был назначен повторный 3-месячный курс мифепристона, после чего зарегистрирован частичный регресс ММ.
Обсуждение результатов
Высокий профиль безопасности и хорошая переносимость выгодно отличают мифепристон от агонистов гонадотропин-рилизинг-гормонов, поскольку он не влияет на минеральную плотность костной ткани и не вызывает других симптомов дефицита эстрогенов [3]. Возможные изменения эндометрия и яичников, связанные с действием мифепристона, носят транзиторный характер, не требуют дополнительных мер и самостоятельно разрешаются после завершения курса лечения [4]. В нашем исследовании после окончания лечения в течение 3-х лет последующий регресс ММ был зарегистрирован у 30,4% пациенток. В течение всего периода наблюдения ни одной из них не потребовалось хирургического лечения, лишь 1 (2,2%) женщине потребовался повторный 3-месячный курс мифепристона.
Возможные негеномные эффекты и эпигенетическая регуляция экспрессии прогестерон-зависимых генов под влиянием мифепристона
Активация рецептора прогестерона (PR) в равной степени усиливает транскрипцию как ростовых (например, гена PCNA), так и проапоптотических факторов (bcl-2), что с учетом диаметрально противоположных клинических эффектов, возможно, предполагает наличие эпигенетических факторов, включая не только профили метилирования промоторных областей генов, но и посттранскрипционное (в основном, реализуемое через микроРНК-эффекты) и посттрансляционное (изменение на уровне третичной структуры протеинов, конъюгирование с небелковыми агентами и др.) регулирование [3]. Продемонстрировано, что клетки миометрия и миомы различаются по экспрессии некоторых микроРНК: miR-21 и miR-26а, участвующих в регуляции скорости роста клеток и активности каспаз [5].
После связывания с лигандами или безлигандной активации через фосфорилирование ядерные PR, кроме соответствующих промоторных областей (PREs), также способны взаимодействовать с другими транскрипционными активаторами (SP1, AP1, FOXO1, p65 субъединицей NF-κB) и внутриклеточными киназами, например MAP-киназного пути. В злокачественно трансформированных клетках был обнаружен негеномный путь действия ядерных PR, активирующий сигнальные каскады EGFR/c-Src/Ras/Erk и PI3K/Akt [6]. Данное внутриклеточное взаимодействие позволяет активировать транскрипционные процессы в генах, не имеющих PRE-промоторов. В настоящее время определены специфические гены, экспрессия которых, в зависимости от набора тканеспецифичных клеточных факторов и/или типа лиганда ядерных PR, может быть активирована или, наоборот, подавлена: гены циклина D1, матриксных металлопротеаз
1, 2, 7, 9, Ets-1, FOXO 1, гликоделина, р21 и р27, а также другие гены, связанные с клеточной адгезией, пролиферативной активностью и особенностями иммунного ответа [7]. Реализуемые через PR негеномные эффекты подтверждаются данными Kovacs K.A. et al., которые выявили повышенные уровни фосфорилирования FOXO1 по Ser256 в клетках миомы, достоверно более высокие, чем в остальном миометрии [8]. По данным Yamagata Y. et al., клетки ММ отличаются по уровням экспрессии ДНК метилтрансфераз (1-го и 3-го типов), которые, в свою очередь, катализируют метилирование нуклеотидных остатков в составе ДНК, т. е. осуществляют эпигенетическое регулирование экспрессии генов [9].
Отсроченные эффекты пролонгированного режима лечения мифепристоном
С осознанием иерархии клеточных популяций макроорганизма предполагается, что изменение профиля экспрессии генов и/или особенности их эпигенетической регуляции способны создавать «прениши» для полипотентных эндометриальных клеток, повышенная миграционная способность которых, в т. ч. обусловленная изменением не только в самих клеточных элементах, но и за счет определенных свойств внеклеточного матрикса и/или особенностями иммунного ответа, может приводить к их транслокации в «пренишу» и формированию пролиферирующего клона лейомиоцитов [10]. Мифепристон, взаимодействуя с PR, способствует их связыванию с набором корепрессоров, тем самым антагонизируя действие прогестерона, что в итоге блокирует транскрипцию прогестерон-зависимых генов и потенциально приводит к изменению уровней экспрессии определенного числа генов и эпигенетических факторов, например микроРНК [11]. При длительном действии SPRM происходит постгеномная модификация участков ДНК, содержащих прогестерон-зависимые гены: метилирование ДНК и деацетилирование гистонов [10]. Подавление экспрессии прогестерон-зависимых генов приводит к ремоделированию внеклеточного матрикса за счет изменения качественного и количественного состава его белков.
Не стоит игнорировать присущие только мифепристону и достигаемые посредством антагонистической активности в отношении глюкокортикоидных рецепторов вероятные иммуномодулирующие эффекты. Мифепристон блокирует вызванное введением интерлейкина (ИЛ)-1β повышение синтеза провоспалительных цитокинов (фактора некроза опухоли α, ИЛ-6) и усиление экспрессии концентраций интегрина MAC-1 (CD11b), нейротрофина p75, каждый из которых способствует пролиферации, дифференцировке и выживанию клеток [12].
Пролонгированный режим приема Гинестрила при лечении миомы матки отличается высоким профилем безопасности и может служить альтернативой хирургическому лечению у определенного контингента пациенток.
Источник

