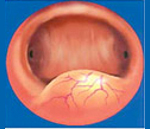
Для миомы матки с узлом характерна
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 ноября 2017;
проверки требуют 13 правок.
Миома матки (также фибромиома, лейомиома) — это доброкачественная опухоль, возникающая в мышечном слое матки — миометрии. Является одним из самых распространенных заболеваний у женщин, достигая частоты 12 — 25% от всех гинекологических заболеваний[1]. Наиболее высокая заболеваемость миомой матки приходится на поздний репродуктивный период и перед климаксом[2]. Существует мнение, что истинная распространенность миомы значительно больше и достигает более 70% как в России, так и за рубежом[1][3].
Узел миомы представляет собой клубок хаотично переплетающихся гладкомышечных волокон округлой формы. Большинство узлов имеют диаметр от нескольких миллиметров до нескольких сантиметров, но иногда они могут достигать больших размеров и веса в несколько килограммов. Так, самый большой узел, о котором имеется упоминание в мировой литературе, весил 63 кг[источник не указан 2034 дня].
Причины появления миомы до конца не изучены. Хотя очевидная роль гормональных факторов в развитии миомы была описана еще в 80-е годы прошлого века в трудах В.М. Бреслера и Г.А. Савицкого[4][5][6], остается неясным вопрос первичности или вторичности миомы по отношению к гормональным сдвигам[7]. Существенную роль играют такие факторы риска, как позднее начало месячных, обильные менструации, медаборты, воспалительные заболевания женских половых органов [1][8]. Другим значимым фактором риска считают избыточную массу тела в сочетании с гиподинамией и стрессами [1][9].
Для лечения миомы матки на протяжении многих десятилетий применяется хирургическое удаление узлов (вылущивание) и даже, во многих случаях крупных узлов, — удаление матки. В настоящее время разработаны эффективные схемы консервативного лечения на основе агонистов ГнРГ, а также эффективные эндоваскулярные методики безоперационного лечения миомы с помощью введения в артерии миомы микроэмболов, перекрывающих кровоток в опухоли[10]. Данные методики позволяют сохранить матку в тех случаях, когда раньше была показана гистерэктомия[11].
Механизм развития[править | править код]
Каждый узел миомы возникает в результате неправильного деления одной гладкомышечной клетки, и поэтому все клетки в узле являются идентичными. Миома матки считается гормонально-зависимой опухолью. Доказательством этого служат следующие факторы:
- обнаружение в опухоли рецепторов к половым гормонам,
- появление миомы в репродуктивном возрасте, когда уровень эстрогенов высокий,
- регресс опухоли после менопаузы, когда уровень эстрогенов достигает минимума,
- появление миомы у некоторых женщин в постменопаузе на фоне приема эстрогенных препаратов.
- механизм гиперэстрогении:
- лейомиомы преобразуют эстрадиол в эстрон;
- клетки лейомиомы содержат большую плотность рецепторов (гормонзависимая опухоль) по сравнению с нормальным миометрием;
- лейомиомы содержат высокие уровни цитохром p450 ароматазы, который позволяет преобразовывать андрогены в эстрогены.
Распространенность[править | править код]
Миома матки — самая распространенная опухоль у женщин. По различным оценкам, она возникает у каждой второй-четвертой женщины в течение репродуктивного периода, преимущественно после 30 лет
.
Классификация[править | править код]
По количеству узлов:
- одиночная миома;
- множественная миома.
По расположению узлов в матке:
- Подслизистые узлы (субмукозная миома) — расположены ближе к полости матки. Встречаются относительно редко, иногда они имеют тонкую ножку и могут опускаться из матки в шейку матки или во влагалище; в этом случае говорят о «рождающемся» узле миомы.
- Межмышечные узлы (интерстициальную, интрамуральную) — узлы находятся в стенке матки в мышечном слое.
- Подбрюшинные узлы (субсерозная миома) — расположены на наружной стороне матки, ближе к брюшной полости. Могут иметь основание меньшего диаметра, чем сам узел; в этом случае употребляют термин «узел на ножке».
- Межсвязочные узлы (интралигаментарная миома).
- Шеечная миома.
Наиболее распространенной является интерстициальная миома матки. По данным разных авторов её частота колеблется от 50 до 61% и более. Частота субсерозной миомы от 26 до 35%, субмукозной не более 13% [12].
В 50% случаев миома матки протекает бессимптомно[13]. Бессимптомное течение более характерно для небольшой одиночной или множественной миомы с межмышечным и подбрюшинным расположением[источник не указан 2026 дней].
Симптомы[править | править код]
Наиболее типичными симптомами миомы матки являются сильные менструальные кровотечения (меноррагии), чувство давления и боли внизу живота. Меноррагии более характерны для подслизистых миом. При росте миомы менструации постепенно становятся более обильными и продолжительными, нередко приводя к развитию малокровия (анемии). Чувство тяжести или давления внизу живота более характерно для межмышечной и подбрюшинной миомы, особенно при больших размерах узлов. Боли, как правило, возникают во время менструаций и носят схваткообразный характер, но могут быть постоянными. Боли также могут иметь внезапный режущий характер, что отмечается при очень редком осложнении — перекруте ножки подбрюшинного узла. К более редким симптомам миомы матки относят бесплодие и нарушение функции соседних органов: мочевого пузыря и прямой кишки.
Диагностика[править | править код]
Для диагностики миомы матки наиболее информативным методом является ультразвуковое исследование, при котором миома обнаруживается в виде округлых очагов пониженной эхогенности (имеющих менее плотную структуру, чем миометрий). В некоторых случаях для дифференциальной диагностики миомы матки и опухоли яичника используют магнитно-резонансную томографию.
Основные методы диагностики миомы матки:
- гинекологический осмотр;
- стандартные гинекологические анализы на микрофлору, цитологию, инфекции;
- анализ крови на гормоны;
- трансвагинальное или трансабдоминальное УЗИ;
- магнитно-резонансная томография (МРТ);
- биопсия.
Лечение[править | править код]
Тактика лечения миомы в значительной мере определяется размерами и количеством узлов, а также степенью выраженности симптомов. При бессимптомных миомах малых размеров часто применяется выжидательная тактика, хотя её оправданность остается спорной [14]. Каким бы малым ни был размер узлов миомы — это точно такое же заболевание, и даже крошечные миоматозные узлы, случайно выявленные во время ультразвукового исследования, должны рассматриваться в качестве терапевтической мишени[15].
Консервативная терапия[править | править код]
Из лекарственных препаратов, использующихся при лечении миомы матки и её симптомов, находят применение следующие:
- Транексамовая кислота. Наиболее эффективное средство при меноррагиях, обусловленных миомой матки. Препарат препятствует разрушению тромбов, блокируя эндометриальный плазминоген. Клинические исследования показывают уменьшение менструальной кровопотери на одну треть.
- Антагонисты гонадотропин релизинг-гормона (ГнРГ). Подавляя выработку гонадотропных гормонов гипофиза, оказывают выраженный антиэстрогенный эффект и вызывают значительное уменьшение размеров узлов миомы. Поскольку эффект агонистов ГнРГ наблюдается только во время использования препаратов, а сроки их применения ограничены побочными эффектами, их используют в основном для подготовки к хирургическому удалению узлов.
Широко назначавшиеся ранее оральные контрацептивы и синтетические прогестагены в клинических исследованиях не обнаружили преимуществ в сравнении с плацебо для торможения роста миомы матки. Так, например, препарат Дюфастон®, часто назначаемый при миоме матки, не только не замедляет, но по некоторым данным ускоряет рост узлов[16].
Хирургическое лечение[править | править код]
До недавнего времени гистерэктомия была единственным методом лечения симптомной миомы. В настоящее время гистерэктомия применяется все реже, уступая место более современным, малотравматичным и высокоэффективным методам[10]. Из эндоскопических методов для удаления подбрюшинных узлов миомы используются лапароскопия, а для удаления подслизистых узлов — гистероскопия.
Эмболизация маточных артерий[править | править код]
Современный метод лечения миомы матки, принцип которого состоит в прекращении кровотока по маточным артериям, и замещении узлов миомы соединительной тканью[17]. Метод заключается в проведении катетера через бедренную артерию в маточную артерию и блокировании в ней кровотока с помощью эмболизационного материала. Процедура выполняется в рентгеноперационной, относится к малоинвазивным вмешательствам и не требует наркоза. Как правило, необходима госпитализация на один день. В настоящее время эмболизация все шире применяется для лечения миомы матки.
ФУЗ-абляция миомы[править | править код]
Метод лечения миомы, основанный на нагревании тканей узлов высокоинтенсивым фокусированным ультразвуком, благодаря передаче большого количества энергии в четко локализованный участок после применения которого наступает деструкция ткани узла — термический некроз. Принцип действия очень напоминает концентрацию солнечных лучей увеличительным стеклом. Вершиной развития метода является на сегодняшний день комбинация источника фокусированного ультразвука (излучатель вмонтированный в стол) и аппарата МРТ. Проведение ультразвука осуществляется через переднюю брюшную стенку. МР томограф контролирует локализацию и что особенно важно температуру нагрева в режиме реального времени. Метод позволяет проводить деструкцию четко ограниченного участка, не повреждая здоровые ткани. Зона между «пролеченной» и здоровой тканью составляет всего лишь несколько рядов клеток. Таким образом фокусированный ультразвук на сегодняшний день как никогда близко приблизился к понятию «идеальный хирургический инструмент» Процедура не требует введения инструментов в полости тела, обезболивания и госпитализации, однако возможна далеко не во всех случаях и требует правильного отбора пациентов. Субстратом для воздействия фокусированного ультразвука является соединительная ткань расположенная в миоме. Соединительная ткань хорошо накапливает энергию и позволяет достичь температуру необходимую для термического некроза. Таким образом очень хорошо лечению методом ФУЗ поддаются так называемые фибромиомы, которые составляют 70% всех миом. Лейомиомы, или клеточные миомы абсолютно не подходят к лечению методом ФУЗ из-за отсутствия субстрата для воздействия и высокоинтенсивному кровоснабжению, что не позволяет провести достаточный нагрев ткани. В период тестирования метода и его внедрения в клиническую практику неправильный отбор пациенток служил причиной частых рецидивов и ошибочно трактовался как неэффективность метода. Для оценки возможности проведения ФУЗ абляции пациентки необходимо пройти МРТ при которой определяется тип миомы. В последнее время многочисленными работами различных авторов [18], основанными на ретроспективных исследованиях пролеченных пациенток, показана высокая эффективность метода, не уступающая по показателям другим методам лечения миомы матки при условии его правильного применения[19][20][21].
Показаниями к применению ФУЗ-абляции в отношении миомы матки являются стандартные показания к органосберегающему лечению при миоме матки. В зависимости от клинических задач, которые ставит врач-гинеколог, применение технологии возможно в четырех тактических вариантах.
1. Органосберегающее лечение миомы матки.
2. Профилактика клинических проявлений миомы матки (что позволяет отказаться от выжидательной амбулаторной практики в отношении роста миоматозных узлов).
3. Подготовка узла миомы к трансцервикальной миомэктомии (в результате FUS-деструкции уменьшаются размеры узла и интенсивность кровотока, что существенно снижает риск возможных осложнений и облегчает проведение операции);
4. С целью отсрочить оперативное лечение.
В отличие от других методов, ФУЗ-МРТ абляция миомы матки — это неинвазивный, органосберегающий метод, без госпитализации, без боли, сохраняет женщине максимально высокие шансы в сравнении с другими методами на успешную беременность, имеет минимальный процент осложнений среди всех используемых методов лечения миомы матки (в настоящее время менее 0,05%).
Метод получил признание во многих странах CE (Европа), FDA (США), MHLW (Japan), CFDA (China), ANVISA (Brazil), Canada FDA, KFDA (Korea), РФ, Тайвань.
Другие виды лечения[править | править код]
Для лечения миомы используются экстракты лекарственных растений и гомеопатические препараты, однако эффективность их не является доказанной.
Профилактика[править | править код]
Специальных мер предупреждения миомы матки не существует.
Примечания[править | править код]
- ↑ 1 2 3 4 Буянова С. Н., Мгелиашвили М. В., Петракова С. А. Современные представления об этиологии, патогенезе и морфогенезе миомы матки //Российский вестник акушера-гинеколога.–2008.–Т. – 2008. – Т. 8. – С. 45-51. (недоступная ссылка)
- ↑ Сидорова И.С. Миома матки (современные аспекты этиологии, патогенеза, классификации и профилактики). В кн.: Миома матки. Под ред. И.С. Сидоровой. М: МИА 2003; 5—66.
- ↑ Мериакри А.В. Эпидемиология и патогенез миомы матки. Сиб мед журн 1998; 2: 8—13.
- ↑ Савицкий Г. А. и др. Локальная гормонемия матки и рецепторы стероидных гормонов //Акушерство и гинекология. – 1985. – №. 2. – С. 19-22.
- ↑ Вихляева Е. М., Савицкий Г. А. Миома матки. Патогенетические и терапевтические аспекты //Акуш. и гин. – 1996. – №. 6. – С. 56.
- ↑ Савицкий Г. А., Иванова Р. Д., Свечникова Ф. А. Роль локальной гипергормонемии в патогенезе темпа прироста массы опухолевых узлов при миоме матки //Акушерство и гинекология. – 1983. – Т. 4. – С. 13-16.
- ↑ Ланчинский В.И., Ищенко А.И. Современные представления об этиологии и патогенезе миомы матки. Вопр гин акуш и перинат 2003; 2: 5—6: 64—69.
- ↑ Вихляева Е.М. Руководство по диагностике и лечению лейомиомы матки. М: МЕДпресс-информ 2004; 400.
- ↑ Рыжова О.О. Патогенетические аспекты роста миоматозных узлов. В кн.: Миома матки. Под ред. И.С. Сидоровой. М: МИА 2002: 98—112.
- ↑ 1 2 Капранов С. А. и др. Новый органосохраняющий метод лечения миомы матки-эмболизация маточных артерий //Лечебное дело. – 2005. – №. 2.
- ↑ Лубнин Д. М., Тихомиров А. Л. Селективная эмболизация маточных артерий в алгоритме органосохраняющего лечения миомы матки : дис. – Москва : [Моск. гос. медико-стоматол. ун-т МЗ РФ], 2005.
- ↑ Медведев М. В., Лютая Е. Д. Миома матки //Допплерография в гинекологии: Энциклопедия ультразвуковой диагностики в акушерстве и гинекологии./Под ред. Зыкина БИ, Медведева МВМ; Реальное время. – 2000. – С. 45-58. (недоступная ссылка)
- ↑ Srividhya Sankaran, Isaac T. Manyonda. Medical management of fibroids. Best Practice & Research Clinical Obstetrics and Gynaecology Vol. 22, No. 4, pp. 655–676, 2008 doi:10.1016/j.bpobgyn.2008.03.001
- ↑ Петракова С. А., Буянова С. Н., Мгелиашвили М. В. Возможности миомэктомии в коррекции репродуктивного здоровья женщин с миомой матки //Российский вестник акушера гинеколога. – 2009. – №. 1. – С. 30-34. (недоступная ссылка). Дата обращения 16 июля 2014. Архивировано 25 июля 2014 года.
- ↑ Андроутопулос Г., Декавалас Г. Последние достижения в лечении миомы матки (недоступная ссылка). Перевод с англ. Н. Д. Фирсовой (2018).
- ↑ Тихомиров А. Д., Лубнин Д. М. Миома матки. Архивная копия от 24 мая 2018 на Wayback Machine 2006, ISBN 5-89481-417-0
- ↑ Б. Ю. Бобров, С. А. Капранов, В. Г. Бреусенко и др. Эмболизация маточных артерий: современный взгляд на проблему. «Диагностическая и интервенционная радиология» том 1 № 2 / 2007
- ↑ Incidence of Additional Treatments in Women Treated with MR-Guided Focused US for Symptomatic Uterine Fibroids: Review of 138 Patients with an Average Follow-up of 2.8 Years Krzysztof R. Gorny, PhD, Bijan J. Borah, PhD, Douglas L. Brown, MD, David A. Woodrum, MD, PhD, Elizabeth A. Stewart, MD, and Gina K. Hesley, MD
- ↑ Gorny KR, Woodrum DA, Brown DL, et al. Magnetic resonance-guided focused ultrasound of uterine leiomyomas: review of a 12-month outcome of 130 clinical patients. J Vasc Interv Radiol 2011; 22:857–864
- ↑ Park Min J, Kim Y, Rhim H, et al. Safety and therapeutic efficacy of complete or near-complete ablation of symptomatic uterine fibroid tumors by MR imaging-guided high intensity focused US therapy. J Vasc Interv Radiol 2014; 25:231–239
- ↑ Лечение больных с миомой матки фокусированным ультразвуком под контролем магнитно-резонанской томографии: клиническая безопасность, возможные осложнения Курашвили Ю.Б, Г.Е Саламандина, Чмыр Е.Н.,О.И. Батаршина., РОССИЙСКИЙ ВЕСТНИК АКУШЕРА-ГИНЕКОЛОГА 2, 2010 стр. 56-60
Ссылки[править | править код]
- Комплексная консервативная терапия миомы матки в сочетании с аденомиозом: применение препарата «Курантил» Consilium medicum
- Патология эндометрия при наличии миомы матки Consilium medicum
- Неоперативные методы лечения миомы матки Медицинский журнал Лечащий врач
Источник

Субмукозная миома — доброкачественная гормонозависимая опухоль, расположенная в подслизистом слое матки и образованная гладкомышечными клетками миометрия. Почти в половине случаев протекает бессимптомно. Может проявляться меноррагиями, нарастающей анемией, схваткообразными болями внизу живота во время менструации, невозможностью забеременеть или выносить ребенка. Для диагностики заболевания используют трансвагинальное УЗИ, гидросонографию, гистероскопию, допплерографию и ангиографию малого таза. В зависимости от особенностей течения выбирают один из методов консервативного, комбинированного, хирургического органосохраняющего или радикального лечения.
Общие сведения
Субмукозную или подслизистую миому (лейомиому) диагностируют в 32% от всех случаев выявления миоматозных узлов. Заболевание поражает женщин репродуктивного возраста и никогда не возникает у девочек до наступления первой менструации. Чаще выявляется у пациенток в возрасте 33-40 лет. В последние годы намечается тенденция к «омоложению» патологии и обнаружению субмукозных узлов у больных 20-25 лет. После наступления климакса подслизистые миомы обычно не развиваются, а уже существующие узлы регрессируют. Существует тесная взаимозависимость между заболеванием и проблемой бесплодия – у каждой пятой женщины, которая не может забеременеть, наличие миоматозных узлов является единственной патологией репродуктивной системы.
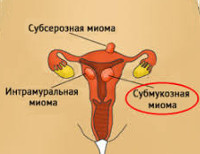
Субмукозная миома матки
Причины субмукозной миомы
Наиболее вероятными причинами возникновения подслизистых узлов являются гормональный дисбаланс и изменение чувствительности гладкомышечных клеток миометрия к действию женских половых гормонов. К развитию субмукозной лейомиомы могут привести:
- Наследственная предрасположенность. Пролиферацию клеток миометрия провоцирует генетически обусловленное изменение их чувствительности к эстрогену и прогестерону.
- Гипоталамо-гипофизарные нарушения. Гормональный дисбаланс возникает при изменении уровня фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормонов. Расстройство может наблюдаться при сосудистых и травматических повреждениях головного мозга, значительных психоэмоциональных нагрузках.
- Изменение эндокринной функции яичников. Уровень секреции эстрогена, прогестерона и нормальное соотношение между этими гормонами нарушается при воспалительных заболеваниях (оофорите, сальпингите, аднексите), травме, опухолях.
- Травматическое повреждение миометрия. Чувствительность гладкомышечных клеток изменяется из-за частых абортов, инвазивных лечебных и диагностических процедур.
- Действие экстрагенитальных факторов. Нарушение выработки женских половых гормонов наблюдается при сахарном диабете, поражении щитовидной железы, некоторых других эндокринных заболеваниях. Уровень эстрогена в крови может повышаться на фоне ожирения, поскольку клетки жировой ткани способны продуцировать этот гормон.
- Неконтролируемый прием гормональных контрацептивов. При длительном использовании контрацептивных препаратов может нарушаться секреция половых гормонов, регулирующих овуляторный цикл.
- Застой в малом тазу. По мнению ряда авторов, причинами гормонального дисбаланса является венозный застой из-за отсутствия регулярной сексуальной разрядки и сидячего образа жизни.
Стоит отметить, что далеко не во всех указанных ситуациях у женщин возникает субмукозная миома. Поэтому поиск пусковых факторов развития заболевания еще продолжается.
Патогенез
Сначала под влиянием провоцирующих факторов вблизи микрососудов в мышечном слое матки формируется активная зона, в клетках которой ускоряются обменные процессы, повышается тканевая проницаемость. В последующем гладкомышечные клетки этой зоны начинают скапливаться в микроскопически и макроскопически определяемые узлы. Со временем чувствительность пролиферирующей ткани к действию гормонов уменьшается, запускаются собственные аутокринопаракринные механизмы роста. Питание субмукозных миом обеспечивают сосуды, утратившие свою адвентициальную оболочку. Растущий подслизистый узел увеличивает площадь отторжения эндометрия и уменьшает способность миометрия к сокращению, что провоцирует более обильные, длительные и болезненные менструальные кровотечения.
Классификация
Подслизистые миомы отличаются количеством узлов, локализацией, размерами и строением. Для классификации заболевания используются следующие критерии:
- Количество узлов. Различают одиночные и множественные субмукозные миомы.
- Размеры. Подслизистые опухоли размером до 20 мм (до 4-5 недель беременности) считаются маленькими, от 20 до 60 мм (от 4-5 до 10-11 недель) – средними, больше 60 мм (12 недель и более) – большими.
- Место расположения. В большинстве случаев новообразования локализуются в теле матки, в 5% – в области шейки.
- Морфология. В зависимости от типа клеток и активности их пролиферации выделяют простые подслизистые миомы, пролиферирующие узлы и предсаркомы.
Симптомы субмукозной миомы
Симптоматика зависит от давности возникновения, размеров и интенсивности роста узла. На начальных этапах симптомы обычно отсутствуют, новообразование становится случайной находкой при гинекологическом осмотре или УЗИ. Первым наиболее характерным признаком роста субмукозного узла является меноррагия — обильное менструальное кровотечение со сгустками крови, длительность которого превышает продолжительность обычной менструации. Кровянистые выделения также могут наблюдаться в межменструальный период. Из-за частных значительных кровопотерь развивается анемия с общим недомоганием, бледностью кожи, головокружениями, головными болями, снижением работоспособности.
Боли при субмукозном расположении узла, по данным специалистов в сфере гинекологии, наблюдаются у 20-50% пациенток. Они обычно возникают во время менструации, носят схваткообразный характер, локализуются в нижней части живота и могут отдавать в поясницу. В отличие от субсерозной миомы, подслизистая опухоль обычно не влияет на расположенные рядом органы. В 10-40% случаев отмечается нарушение репродуктивной функции – невозможность забеременеть или самопроизвольное прерывание беременности.
Осложнения
Субмукозная миома может осложняться массивными маточными кровотечениями, развитием выраженной анемии. При значительной деформации полости матки возрастает риск бесплодия, выкидышей, патологической беременности и родов. В 7-16% случаев узел подвергается сухому или влажному некрозу. При наличии восходящей инфекции подслизистая миома может нагноиться или абсцедировать, при этом у пациентки повышается температура, возникает озноб, боли внизу живота, изменяется общее состояние. Наиболее грозным осложнением является «рождение» подслизистого узла, которое сопровождается «кинжальными» схваткообразными болями внизу живота, кровотечением, риском инфицирования. Злокачественное перерождение опухоли отмечается редко (в 1,5-3% случаев заболевания).
Диагностика
Поскольку клиническая симптоматика при субмукозной миоме неспецифична и выражена не у всех пациенток, важную роль в диагностике играют физикальные и инструментальные исследования. В план обследования обычно включают:
- Осмотр гинеколога. При бимануальной пальпации выявляется увеличенная матка.
- Трансвагинальное УЗИ, гидросонографию, допплерографию. Методики позволяют определить размеры, тип и структуру узлов, выявить патологию эндометрия, оценить толщину гладкомышечного слоя и интенсивность кровотока.
- Гистероскопию. В матке обнаруживают овальное или округлое образование с гладкой бледно-розовой поверхностью либо множественные узлы на ножках, свисающие в виде «гроздьев» в ее полость.
- Ангиографию органов малого таза. Визуализация кровеносной системы матки дает возможность подтвердить отсутствие неоваскуляризации своевременно дифференцировать доброкачественный узел от злокачественной неоплазии.
- Рентгенотелевизионную гистеросальпингографию. Выявляет изменение формы полости матки с участками просветления или дефектами наполнения. В настоящее время применяется редко.
- МРТ и КТ матки. Методы применяются для точной оценки топографии миоматозных узлов.
Поскольку для субмукозной миомы характерно развитие анемии, в общем анализе крови часто обнаруживается эритропения и снижение уровня гемоглобина. Заболевание необходимо дифференцировать от беременности, полипов, саркомы, внутреннего эндометриоза тела матки. При необходимости к обследованию привлекают онкогинеколога, эндокринолога.
Лечение субмукозной миомы
При выборе врачебной тактики учитывают возраст женщины, ее планы по сохранению репродуктивной функции, размеры, расположение и интенсивность роста узлов, выраженность клинической картины и наличие осложнений. Пациенткам с новообразованиями стабильных размеров при отсутствии меноррагий, болевого синдрома, сохраненной репродуктивной функции рекомендовано динамическое наблюдение с ежегодным осмотром гинеколога. В остальных случаях выбирают один из способов консервативного, комбинированного или хирургического лечения.
Медикаментозная терапия показана при опухолях размерами до 3 см, умеренных меноррагиях, медленном росте новообразований. Больным рекомендованы препараты, которые угнетают секрецию женских половых гормонов, устраняя одну из основных причин образования опухоли — гормональную стимуляцию роста. Такую терапию обычно дополняют симптоматическими средствами. Особенно эффективно консервативное лечение в пременопаузе, которая сменяется естественной менопаузой. Как правило, пациенткам назначают:
- Препараты, угнетающие секрецию гонадотропинов. При использовании антигонадотропинов и агонистов гонадотропных рилизинг-гормонов (А-ГнРТ) размеры узлов стабилизируются или даже уменьшаются, а кровопотеря при менструациях снижается.
- Оральные или внутриматочные гормональные контрацептивы. Показаны женщинам детородного возраста для стабилизации эффекта, достигнутого при угнетении секреции гонадотропинов.
- Гемостатики и препараты, сокращающие матку. Применяются для уменьшения кровопотери при меноррагиях.
- Общеукрепляющие средства. Для улучшения общего самочувствия назначаются витаминно-минеральные комплексы и препараты железа.
Комбинированное лечение – оптимальный вариант для пациенток, которые хотят сохранить репродуктивную функцию при наличии единичного узла или множественных образований размером от 50 мм с клинической симптоматикой и тенденцией к медленному росту. При этом методе назначение А-ГнРТ предваряет и завершает консервативную миомэктомию. Использование гормональных препаратов накануне вмешательства позволяет уменьшить размеры доброкачественных подслизистых узлов, снизить кровопотерю, сократить продолжительность операции и послеоперационного восстановления.
Хирургическое лечение рекомендовано, если узел достигает больших размеров (от 12 недель беременности), интенсивно растет (увеличение на 4-5 и более недель за год, особенно во время климакса и менопаузы), сопровождается нарастающей анемией, болями и развитием осложнений (в том числе бесплодия). В зависимости от течения заболевания и репродуктивных планов женщины могут быть выбраны следующие виды вмешательств:
- Органосохраняющие операции. Миоматозные узлы удаляют методом гистерорезектоскопии (трансцервикальной миомэктомии) с использованием механических, лазеро- или электрохирургических инструментов либо разрушают при помощи высокочастотного фокусированного ультразвукового воздействия (ФУЗ-абляции) или криомиолиза. Эмболизация маточных артерий позволяет ограничить питание опухоли и привести к ее рассасыванию.
- Радикальные вмешательства. При неблагоприятном течении заболевания женщине рекомендуют трансвагинальную, лапароскопическую, лапаротомическую дефундацию матки, субтотальную (надвлагалищную) или тотальную гистерэктомию.
Прогноз и профилактика
При своевременном выявлении и адекватном лечении прогноз субмукозной миомы благоприятный. В период менопаузы опухоль, как правило, регрессирует. Эффективность эмболизации маточных артерий составляет до 50%. Проведение органосохраняющих вмешательств позволяет восстановить репродуктивную функцию у женщин детородного возраста. Послеоперационный период в зависимости от объема операции и вида доступа длится от 7 до 24 дней. Срок диспансерного наблюдения после гистерэктомии составляет 5 лет, После миомэктомии из-за возможности развития рецидива женщины наблюдаются пожизненно. Основными методами профилактики заболевания являются рациональное назначение гормональных контрацептивов, ограничение инвазивных вмешательств, лечение заболеваний, при которых наблюдается гиперэстрогенемия.
Источник


