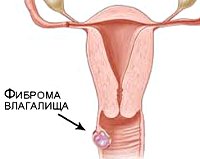
Миомы матки во влагалище
Доброкачественные опухоли влагалища – дополнительные образования влагалищной трубки, развивающиеся из структур соединительной ткани, эпителия, сосудов. Течение доброкачественных опухолей влагалища чаще бессимптомное; при увеличении в размерах опухоли могут вызывать ощущения инородного тела, дискомфорт при половом сношении, нарушения дефекации и мочеиспускания. Опухоли влагалища диагностируются в ходе гинекологического осмотра, кольпоскопии, трансвагинального УЗИ. Доброкачественные опухоли влагалища подлежат оперативному удалению.
Общие сведения
Из доброкачественных опухолей влагалища клиническая гинекология сталкивается с кистами, фибромами, миомами, липомами, папилломами, гемангиомами. Происхождение доброкачественных опухолей влагалища полиэтиологично; в их развитии предполагается определенная роль нарушений нейроэндокринной регуляции, воздействия вирусов, рецидивирующих кольпитов. Доброкачественные опухоли влагалища чаще обнаруживаются у пациенток в возрасте 20-50 лет. Необходимость хирургической тактики в отношении опухолей влагалища диктуется возможностью их нагноения, некроза, реже – злокачественного перерождения.

Доброкачественные опухоли влагалища
Доброкачественные опухоли влагалища: симптомы, диагностика, лечение
Фиброма, миома, липома влагалища
К истинным доброкачественным опухолям влагалища относятся фибромы, миомы, фибромиомы, липомы. В основе роста доброкачественных опухолей влагалища лежит пролиферация соединительной (фиброма), гладкомышечной (миома), реже жировой (липома) ткани. Истинные опухоли локализуются под слизистой влагалищной стенки; могут иметь вид одиночного узла с широким основанием или длинной ножкой; реже носят характер множественных узелков.
Клинически опухоли влагалища могут проявлять себя тянущими или контактными болями, ощущением инородного тела, дискомфортом при половом контакте, нарушениями дефекации и мочеиспускания. Перекрут ножки или кровоизлияние в ткани опухоли влагалища может сопровождаться некротизированием, воспалением или нагноением. В редких случаях наблюдается малигнизация доброкачественных опухолей влагалища.
Истинные опухоли влагалища обнаруживаются в ходе гинекологического осмотра. При бимануальном исследовании пальпируется опухоль, связанная со стенкой влагалища, имеющая четкие границы, плотную консистенцию, ограниченную подвижность. При осмотре в зеркалах обнаруживается узел, располагающийся в области передней стенки, на широком основании или ножке под неизмененной слизистой влагалища. Величина истинных опухолей влагалища может достигать куриного яйца. В процессе трансвагинального УЗИ визуализируется солидная структура опухолей влагалища, средняя или пониженная эхогенность, аналогичная фибромиоме матки.
При бессимптомных опухолях влагалища за ними может быть установлено динамическое наблюдение. При тенденции к росту или клинической симтоматике опухоли влагалища удаляются оперативным способом: производится их вылущивание из подслизистого слоя в пределах ложа или отсечение ножки. Операция чаще выполняется чрезвлагалищным доступом; глубоко расположенные опухоли влагалища могут удаляться с применением брюшностеночного чревосечения. Морфологическая форма опухоли влагалища устанавливается в процессе гистологического исследования препарата.
Папилломы (кондиломы) влагалища
Папилломы (кондиломы) – это опухоли покровного эпителия, имеющие вид сосочковых разрастаний на слизистой влагалища. Папилломы служат проявлением общей папилломавирусной инфекции. Обладают экзофитным ростом, имеют тонкую ножку или широкое основание. Папилломы могут проявляться зудом, жжением во влагалище, контактными кровотечениями при травматизации, необычными выделениями. Папилломатозные опухоли влагалища в ряде случаев подвергаются распаду или малигнизации.
Диагностика папиллом включает цитологическое исследование мазка, проведение кольпоскопии, биопсию опухоли влагалища с гистологическим исследованием, ПЦР-определение ВПЧ с типированием неонкогенных и онкогенных штаммов.
Удаление папиллом влагалища строго обязательно и может производиться медикаментозно, жидким азотом, лазером, электрокоагуляцией, плазменной коагуляцией, хирургическим скальпелем, радиоволновым методом. После удаления папиллом назначается иммуномодулирующая терапия.
Гемангиома влагалища
Гемангиомы – сосудистые опухоли влагалища с мягкой консистенцией. По структуре различают капиллярные и кавернозные гемангиомы. Возникнув на слизистой влагалища, гемангиомы могут распространяться на цервикальный канал и в полость матки. В некоторых случаях отмечается изъязвление и некроз сосудистых опухолей влагалища.
Гемангиомы влагалища чаще проявляют себя контактными кровотечениями при травматизации. При распространении сосудистой опухоли влагалища на внутренние гениталии может возникать клиника гиперполименореи.
При гинекологическом осмотре гемангиома влагалища имеет вид красного, пурпурного или синюшного пятна, возвышающегося над слизистой. Отмечается местная отечность слизистой, разрыхление покровного эпителия, нагрубание складок. При кольпоскопии обращает внимание наличие обширной сети анастомозирующих, на некоторых участках – варикозно измененных сосудов.
Непрогрессирующие, неизъязвляющиеся, не нарушающие овариально-менструальный цикл сосудистые опухоли влагалища могут быть оставлены под наблюдение. При прогрессирующей клинике гемангиомы влагалища могут быть удалены хирургически, методами криотерапии, электрокоагуляции, путем склеротерапии.
Прогноз при доброкачественных опухолях влагалища
Несмотря на то, что озлокачествление неудаленных доброкачественных опухолей влагалища происходит нечасто, оптимальной тактикой в их отношении является радикальное иссечение в пределах границ неизмененных тканей. Рецидивы после удаления опухолей влагалища возникают редко.
Наличие опухоли влагалища является отягощающим фактором течения беременности, поскольку может препятствовать нормальным родам, провоцировать дискоординированную родовую деятельность, кровотечение. Ведение беременности у женщин с доброкачественной опухолью влагалища требует динамического отслеживания состояния новообразования и заблаговременного выбора способа родоразрешения.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 ноября 2017;
проверки требуют 13 правок.
Миома матки (также фибромиома, лейомиома) — это доброкачественная опухоль, возникающая в мышечном слое матки — миометрии. Является одним из самых распространенных заболеваний у женщин, достигая частоты 12 — 25% от всех гинекологических заболеваний[1]. Наиболее высокая заболеваемость миомой матки приходится на поздний репродуктивный период и перед климаксом[2]. Существует мнение, что истинная распространенность миомы значительно больше и достигает более 70% как в России, так и за рубежом[1][3].
Узел миомы представляет собой клубок хаотично переплетающихся гладкомышечных волокон округлой формы. Большинство узлов имеют диаметр от нескольких миллиметров до нескольких сантиметров, но иногда они могут достигать больших размеров и веса в несколько килограммов. Так, самый большой узел, о котором имеется упоминание в мировой литературе, весил 63 кг[источник не указан 2025 дней].
Причины появления миомы до конца не изучены. Хотя очевидная роль гормональных факторов в развитии миомы была описана еще в 80-е годы прошлого века в трудах В.М. Бреслера и Г.А. Савицкого[4][5][6], остается неясным вопрос первичности или вторичности миомы по отношению к гормональным сдвигам[7]. Существенную роль играют такие факторы риска, как позднее начало месячных, обильные менструации, медаборты, воспалительные заболевания женских половых органов [1][8]. Другим значимым фактором риска считают избыточную массу тела в сочетании с гиподинамией и стрессами [1][9].
Для лечения миомы матки на протяжении многих десятилетий применяется хирургическое удаление узлов (вылущивание) и даже, во многих случаях крупных узлов, — удаление матки. В настоящее время разработаны эффективные схемы консервативного лечения на основе агонистов ГнРГ, а также эффективные эндоваскулярные методики безоперационного лечения миомы с помощью введения в артерии миомы микроэмболов, перекрывающих кровоток в опухоли[10]. Данные методики позволяют сохранить матку в тех случаях, когда раньше была показана гистерэктомия[11].
Механизм развития[править | править код]
Каждый узел миомы возникает в результате неправильного деления одной гладкомышечной клетки, и поэтому все клетки в узле являются идентичными. Миома матки считается гормонально-зависимой опухолью. Доказательством этого служат следующие факторы:
- обнаружение в опухоли рецепторов к половым гормонам,
- появление миомы в репродуктивном возрасте, когда уровень эстрогенов высокий,
- регресс опухоли после менопаузы, когда уровень эстрогенов достигает минимума,
- появление миомы у некоторых женщин в постменопаузе на фоне приема эстрогенных препаратов.
- механизм гиперэстрогении:
- лейомиомы преобразуют эстрадиол в эстрон;
- клетки лейомиомы содержат большую плотность рецепторов (гормонзависимая опухоль) по сравнению с нормальным миометрием;
- лейомиомы содержат высокие уровни цитохром p450 ароматазы, который позволяет преобразовывать андрогены в эстрогены.
Распространенность[править | править код]
Миома матки — самая распространенная опухоль у женщин. По различным оценкам, она возникает у каждой второй-четвертой женщины в течение репродуктивного периода, преимущественно после 30 лет
.
Классификация[править | править код]
По количеству узлов:
- одиночная миома;
- множественная миома.
По расположению узлов в матке:
- Подслизистые узлы (субмукозная миома) — расположены ближе к полости матки. Встречаются относительно редко, иногда они имеют тонкую ножку и могут опускаться из матки в шейку матки или во влагалище; в этом случае говорят о «рождающемся» узле миомы.
- Межмышечные узлы (интерстициальную, интрамуральную) — узлы находятся в стенке матки в мышечном слое.
- Подбрюшинные узлы (субсерозная миома) — расположены на наружной стороне матки, ближе к брюшной полости. Могут иметь основание меньшего диаметра, чем сам узел; в этом случае употребляют термин «узел на ножке».
- Межсвязочные узлы (интралигаментарная миома).
- Шеечная миома.
Наиболее распространенной является интерстициальная миома матки. По данным разных авторов её частота колеблется от 50 до 61% и более. Частота субсерозной миомы от 26 до 35%, субмукозной не более 13% [12].
В 50% случаев миома матки протекает бессимптомно[13]. Бессимптомное течение более характерно для небольшой одиночной или множественной миомы с межмышечным и подбрюшинным расположением[источник не указан 2017 дней].
Симптомы[править | править код]
Наиболее типичными симптомами миомы матки являются сильные менструальные кровотечения (меноррагии), чувство давления и боли внизу живота. Меноррагии более характерны для подслизистых миом. При росте миомы менструации постепенно становятся более обильными и продолжительными, нередко приводя к развитию малокровия (анемии). Чувство тяжести или давления внизу живота более характерно для межмышечной и подбрюшинной миомы, особенно при больших размерах узлов. Боли, как правило, возникают во время менструаций и носят схваткообразный характер, но могут быть постоянными. Боли также могут иметь внезапный режущий характер, что отмечается при очень редком осложнении — перекруте ножки подбрюшинного узла. К более редким симптомам миомы матки относят бесплодие и нарушение функции соседних органов: мочевого пузыря и прямой кишки.
Диагностика[править | править код]
Для диагностики миомы матки наиболее информативным методом является ультразвуковое исследование, при котором миома обнаруживается в виде округлых очагов пониженной эхогенности (имеющих менее плотную структуру, чем миометрий). В некоторых случаях для дифференциальной диагностики миомы матки и опухоли яичника используют магнитно-резонансную томографию.
Основные методы диагностики миомы матки:
- гинекологический осмотр;
- стандартные гинекологические анализы на микрофлору, цитологию, инфекции;
- анализ крови на гормоны;
- трансвагинальное или трансабдоминальное УЗИ;
- магнитно-резонансная томография (МРТ);
- биопсия.
Лечение[править | править код]
Тактика лечения миомы в значительной мере определяется размерами и количеством узлов, а также степенью выраженности симптомов. При бессимптомных миомах малых размеров часто применяется выжидательная тактика, хотя её оправданность остается спорной [14]. Каким бы малым ни был размер узлов миомы — это точно такое же заболевание, и даже крошечные миоматозные узлы, случайно выявленные во время ультразвукового исследования, должны рассматриваться в качестве терапевтической мишени[15].
Консервативная терапия[править | править код]
Из лекарственных препаратов, использующихся при лечении миомы матки и её симптомов, находят применение следующие:
- Транексамовая кислота. Наиболее эффективное средство при меноррагиях, обусловленных миомой матки. Препарат препятствует разрушению тромбов, блокируя эндометриальный плазминоген. Клинические исследования показывают уменьшение менструальной кровопотери на одну треть.
- Антагонисты гонадотропин релизинг-гормона (ГнРГ). Подавляя выработку гонадотропных гормонов гипофиза, оказывают выраженный антиэстрогенный эффект и вызывают значительное уменьшение размеров узлов миомы. Поскольку эффект агонистов ГнРГ наблюдается только во время использования препаратов, а сроки их применения ограничены побочными эффектами, их используют в основном для подготовки к хирургическому удалению узлов.
Широко назначавшиеся ранее оральные контрацептивы и синтетические прогестагены в клинических исследованиях не обнаружили преимуществ в сравнении с плацебо для торможения роста миомы матки. Так, например, препарат Дюфастон®, часто назначаемый при миоме матки, не только не замедляет, но по некоторым данным ускоряет рост узлов[16].
Хирургическое лечение[править | править код]
До недавнего времени гистерэктомия была единственным методом лечения симптомной миомы. В настоящее время гистерэктомия применяется все реже, уступая место более современным, малотравматичным и высокоэффективным методам[10]. Из эндоскопических методов для удаления подбрюшинных узлов миомы используются лапароскопия, а для удаления подслизистых узлов — гистероскопия.
Эмболизация маточных артерий[править | править код]
Современный метод лечения миомы матки, принцип которого состоит в прекращении кровотока по маточным артериям, и замещении узлов миомы соединительной тканью[17]. Метод заключается в проведении катетера через бедренную артерию в маточную артерию и блокировании в ней кровотока с помощью эмболизационного материала. Процедура выполняется в рентгеноперационной, относится к малоинвазивным вмешательствам и не требует наркоза. Как правило, необходима госпитализация на один день. В настоящее время эмболизация все шире применяется для лечения миомы матки.
ФУЗ-абляция миомы[править | править код]
Метод лечения миомы, основанный на нагревании тканей узлов высокоинтенсивым фокусированным ультразвуком, благодаря передаче большого количества энергии в четко локализованный участок после применения которого наступает деструкция ткани узла — термический некроз. Принцип действия очень напоминает концентрацию солнечных лучей увеличительным стеклом. Вершиной развития метода является на сегодняшний день комбинация источника фокусированного ультразвука (излучатель вмонтированный в стол) и аппарата МРТ. Проведение ультразвука осуществляется через переднюю брюшную стенку. МР томограф контролирует локализацию и что особенно важно температуру нагрева в режиме реального времени. Метод позволяет проводить деструкцию четко ограниченного участка, не повреждая здоровые ткани. Зона между «пролеченной» и здоровой тканью составляет всего лишь несколько рядов клеток. Таким образом фокусированный ультразвук на сегодняшний день как никогда близко приблизился к понятию «идеальный хирургический инструмент» Процедура не требует введения инструментов в полости тела, обезболивания и госпитализации, однако возможна далеко не во всех случаях и требует правильного отбора пациентов. Субстратом для воздействия фокусированного ультразвука является соединительная ткань расположенная в миоме. Соединительная ткань хорошо накапливает энергию и позволяет достичь температуру необходимую для термического некроза. Таким образом очень хорошо лечению методом ФУЗ поддаются так называемые фибромиомы, которые составляют 70% всех миом. Лейомиомы, или клеточные миомы абсолютно не подходят к лечению методом ФУЗ из-за отсутствия субстрата для воздействия и высокоинтенсивному кровоснабжению, что не позволяет провести достаточный нагрев ткани. В период тестирования метода и его внедрения в клиническую практику неправильный отбор пациенток служил причиной частых рецидивов и ошибочно трактовался как неэффективность метода. Для оценки возможности проведения ФУЗ абляции пациентки необходимо пройти МРТ при которой определяется тип миомы. В последнее время многочисленными работами различных авторов [18], основанными на ретроспективных исследованиях пролеченных пациенток, показана высокая эффективность метода, не уступающая по показателям другим методам лечения миомы матки при условии его правильного применения[19][20][21].
Показаниями к применению ФУЗ-абляции в отношении миомы матки являются стандартные показания к органосберегающему лечению при миоме матки. В зависимости от клинических задач, которые ставит врач-гинеколог, применение технологии возможно в четырех тактических вариантах.
1. Органосберегающее лечение миомы матки.
2. Профилактика клинических проявлений миомы матки (что позволяет отказаться от выжидательной амбулаторной практики в отношении роста миоматозных узлов).
3. Подготовка узла миомы к трансцервикальной миомэктомии (в результате FUS-деструкции уменьшаются размеры узла и интенсивность кровотока, что существенно снижает риск возможных осложнений и облегчает проведение операции);
4. С целью отсрочить оперативное лечение.
В отличие от других методов, ФУЗ-МРТ абляция миомы матки — это неинвазивный, органосберегающий метод, без госпитализации, без боли, сохраняет женщине максимально высокие шансы в сравнении с другими методами на успешную беременность, имеет минимальный процент осложнений среди всех используемых методов лечения миомы матки (в настоящее время менее 0,05%).
Метод получил признание во многих странах CE (Европа), FDA (США), MHLW (Japan), CFDA (China), ANVISA (Brazil), Canada FDA, KFDA (Korea), РФ, Тайвань.
Другие виды лечения[править | править код]
Для лечения миомы используются экстракты лекарственных растений и гомеопатические препараты, однако эффективность их не является доказанной.
Профилактика[править | править код]
Специальных мер предупреждения миомы матки не существует.
Примечания[править | править код]
- ↑ 1 2 3 4 Буянова С. Н., Мгелиашвили М. В., Петракова С. А. Современные представления об этиологии, патогенезе и морфогенезе миомы матки //Российский вестник акушера-гинеколога.–2008.–Т. – 2008. – Т. 8. – С. 45-51. (недоступная ссылка)
- ↑ Сидорова И.С. Миома матки (современные аспекты этиологии, патогенеза, классификации и профилактики). В кн.: Миома матки. Под ред. И.С. Сидоровой. М: МИА 2003; 5—66.
- ↑ Мериакри А.В. Эпидемиология и патогенез миомы матки. Сиб мед журн 1998; 2: 8—13.
- ↑ Савицкий Г. А. и др. Локальная гормонемия матки и рецепторы стероидных гормонов //Акушерство и гинекология. – 1985. – №. 2. – С. 19-22.
- ↑ Вихляева Е. М., Савицкий Г. А. Миома матки. Патогенетические и терапевтические аспекты //Акуш. и гин. – 1996. – №. 6. – С. 56.
- ↑ Савицкий Г. А., Иванова Р. Д., Свечникова Ф. А. Роль локальной гипергормонемии в патогенезе темпа прироста массы опухолевых узлов при миоме матки //Акушерство и гинекология. – 1983. – Т. 4. – С. 13-16.
- ↑ Ланчинский В.И., Ищенко А.И. Современные представления об этиологии и патогенезе миомы матки. Вопр гин акуш и перинат 2003; 2: 5—6: 64—69.
- ↑ Вихляева Е.М. Руководство по диагностике и лечению лейомиомы матки. М: МЕДпресс-информ 2004; 400.
- ↑ Рыжова О.О. Патогенетические аспекты роста миоматозных узлов. В кн.: Миома матки. Под ред. И.С. Сидоровой. М: МИА 2002: 98—112.
- ↑ 1 2 Капранов С. А. и др. Новый органосохраняющий метод лечения миомы матки-эмболизация маточных артерий //Лечебное дело. – 2005. – №. 2.
- ↑ Лубнин Д. М., Тихомиров А. Л. Селективная эмболизация маточных артерий в алгоритме органосохраняющего лечения миомы матки : дис. – Москва : [Моск. гос. медико-стоматол. ун-т МЗ РФ], 2005.
- ↑ Медведев М. В., Лютая Е. Д. Миома матки //Допплерография в гинекологии: Энциклопедия ультразвуковой диагностики в акушерстве и гинекологии./Под ред. Зыкина БИ, Медведева МВМ; Реальное время. – 2000. – С. 45-58. (недоступная ссылка)
- ↑ Srividhya Sankaran, Isaac T. Manyonda. Medical management of fibroids. Best Practice & Research Clinical Obstetrics and Gynaecology Vol. 22, No. 4, pp. 655–676, 2008 doi:10.1016/j.bpobgyn.2008.03.001
- ↑ Петракова С. А., Буянова С. Н., Мгелиашвили М. В. Возможности миомэктомии в коррекции репродуктивного здоровья женщин с миомой матки //Российский вестник акушера гинеколога. – 2009. – №. 1. – С. 30-34. (недоступная ссылка). Дата обращения 16 июля 2014. Архивировано 25 июля 2014 года.
- ↑ Андроутопулос Г., Декавалас Г. Последние достижения в лечении миомы матки (недоступная ссылка). Перевод с англ. Н. Д. Фирсовой (2018).
- ↑ Тихомиров А. Д., Лубнин Д. М. Миома матки. Архивная копия от 24 мая 2018 на Wayback Machine 2006, ISBN 5-89481-417-0
- ↑ Б. Ю. Бобров, С. А. Капранов, В. Г. Бреусенко и др. Эмболизация маточных артерий: современный взгляд на проблему. «Диагностическая и интервенционная радиология» том 1 № 2 / 2007
- ↑ Incidence of Additional Treatments in Women Treated with MR-Guided Focused US for Symptomatic Uterine Fibroids: Review of 138 Patients with an Average Follow-up of 2.8 Years Krzysztof R. Gorny, PhD, Bijan J. Borah, PhD, Douglas L. Brown, MD, David A. Woodrum, MD, PhD, Elizabeth A. Stewart, MD, and Gina K. Hesley, MD
- ↑ Gorny KR, Woodrum DA, Brown DL, et al. Magnetic resonance-guided focused ultrasound of uterine leiomyomas: review of a 12-month outcome of 130 clinical patients. J Vasc Interv Radiol 2011; 22:857–864
- ↑ Park Min J, Kim Y, Rhim H, et al. Safety and therapeutic efficacy of complete or near-complete ablation of symptomatic uterine fibroid tumors by MR imaging-guided high intensity focused US therapy. J Vasc Interv Radiol 2014; 25:231–239
- ↑ Лечение больных с миомой матки фокусированным ультразвуком под контролем магнитно-резонанской томографии: клиническая безопасность, возможные осложнения Курашвили Ю.Б, Г.Е Саламандина, Чмыр Е.Н.,О.И. Батаршина., РОССИЙСКИЙ ВЕСТНИК АКУШЕРА-ГИНЕКОЛОГА 2, 2010 стр. 56-60
Ссылки[править | править код]
- Комплексная консервативная терапия миомы матки в сочетании с аденомиозом: применение препарата «Курантил» Consilium medicum
- Патология эндометрия при наличии миомы матки Consilium medicum
- Неоперативные методы лечения миомы матки Медицинский журнал Лечащий врач
Источник


