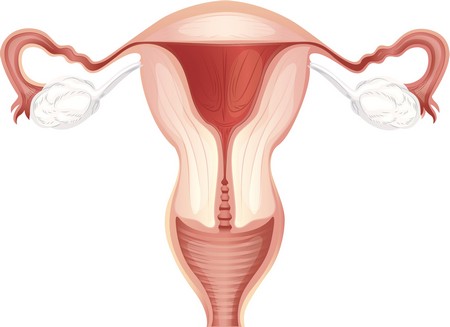
Разрастание миом на матке

08 февраль 2018
 13540
13540
 0
0
 Гиперплазия эндометрия, миома матки – гинекологические заболевания, которые могут стать причиной бесплодия женщины. Гиперпластические процессы в мукозном слое могут стать причиной развития злокачественного новообразования матки.
Гиперплазия эндометрия, миома матки – гинекологические заболевания, которые могут стать причиной бесплодия женщины. Гиперпластические процессы в мукозном слое могут стать причиной развития злокачественного новообразования матки.
Обращаем ваше внимание, что данный текст готовился без поддержки нашего Экспертного совета.
1
Что означает: миома матки с эндометрия гиперплазией
Миома, эндометрия гиперплазия – это два разных гормоночувствительных заболевания, которые осложняют течение друг друга. Миома матки с гиперплазией эндометрия нередко становится причиной развития бесплодия у женщины. Заболевания длительное время протекают без выраженной симптоматики, пока не переходят в более тяжелую стадию. Чтобы избежать развития осложнений при миоме и гиперплазии, следует своевременно обращаться к врачу, регулярно проходить профилактический осмотр у гинеколога. Получить исчерпывающие ответы вам поможет консультация по e-mail. Опытные врачи дадут рекомендации, расскажут какой вид диагностики вам надо пройти, какие методы лечения применяют в клинике.
Эндометрий – это внутренний слизистый (мукозный) слой матки, который имеет сложное строение. Нижняя часть слоя называется базальной, верхняя – функциональной. Функциональный слой имеет большое количество гормоночувствительных рецепторов, постоянно изменяется в зависимости от фазы менструального цикла. В самом начале менструального цикла функциональный слой очень тонкий, затем под действием гормонов толщина слизистого слоя начинает увеличиваться и к моменту выхода яйцеклетки приобретает нужную толщину, которая способствует прикреплению эмбриона к стенке матки. Если после выхода из фолликула яйцеклетка не оплодотворилась, то функциональный слой отторгается – начинается менструация. Базальный слой обеспечивает восстановление отторгнутого функционального слоя в следующем менструальном цикле.
После менструации происходит восстановление функционального слоя и процесс повторяется. Все эти процессы регулируются гормональной системой. На изменение функционального слоя оказывают свое влияние прогестероны и эстрогены. Вырабатываемые организмом эстрогены вызывают рост толщины эндометрия, готовят его к беременности, в определенное время организм начинает продуцировать больше прогестерона и он останавливает рост толщины эндометрия, регулирует ее. Такой слаженный процесс возможен при хорошей работе эндокринных органов, балансе гормонов. Когда происходит нарушение баланса гормонов, это приводит к нарушению менструального цикла, снижению шанса на беременность, развитию заболеваний матки.
Повышение уровня эстрогенов и снижение прогестерона приводит к неконтролируемому росту толщины эндометрия, развитию эндометриоза; снижение уровня эстрогенов и повышение прогестерона не дает возможности увеличиваться толщине слизистого слоя в определенное время менструального цикла. Не создаются условия для прикрепления оплодотворенной яйцеклетки к стенке матки, беременность не наступает. Недостаток прогестерона в конце менструального цикла также не позволяет контролировать рост толщины слизистого слоя. В результате дисбаланса гормонов нарушается менструальный цикл, менструации могут быть нерегулярными, а когда менструация начинается, она сопровождается сильной болью, становится длительной, обильной.
3
Причины развития гиперпластических процессов в эндометрии
Гиперплазия эндометрия – это заболевание, которое сопровождает периоды гормональной перестройки организма. Наиболее часто патологию обнаруживают во время полового созревания и в предклимактерическом периоде. При появлении признаков заболевания следует записаться на приём
- Заболевания эндокринной системы (заболевания щитовидной железы, сахарный диабет).
- Синдром резистентности к инсулину, сопровождающийся ожирением и высоким артериальным давлением.
- Эндометрит (хроническая форма).
- Миома матки (интерстициальная).
- Генитальный эндометриоз.
- Синдром поликистоза яичников.
- Бесплодие, в течение длительного времени не поддающееся лечению.
- Наследственная предрасположенность.
- Нарушение иммунитета.
- Заболевания печени.
- Врожденные дефекты матки.
Длительное течение заболевания при отсутствии адекватного лечения приводит к раку эндометрия, провоцирующими факторами являются:
- Сахарный диабет.
- Ожирение и артериальная гипертензия.
- Синдром поликистоза яичников.
- Длительное нарушение менструального цикла.
- Бесплодие.
4
Диагностика гиперплазии эндометрия
Диагностика гиперплазии мукозного слоя матки проходит с помощью УЗИ, МРТ, гистероскопии и лабораторных анализов на уровень гормонов в крови. Самый распространенный метод исследования – это ультразвуковое исследование органов малого таза. С помощью современного оборудования можно очень точно определить толщину слизистого слоя. УЗИ для диагностики патологии проводится в середине менструального цикла или сразу по окончанию менструации.
Гистероскопия позволяет провести исследование ткани эндометрия с помощью биопсии. Информативность исследования составляет от 60 до 97%. Полиповидная форма гиперплазии при гистероскопии видна как разрастания полиповидного эндометрия бледного цвета с розовым оттенком, на поверхности множественные эндометриальные синехии и пузырьки. Слизистый слой выглядит неровным, содержит кисты, углубления, различные борозды. При исследовании матки во время отсутствия выделений крови гиперплазированный эндометрий выглядит в виде утолщенных складок, с большим количеством протоков желез, отечный, бледно-розовый. При исследовании во время длительных менструальных выделений он тонкий и бледный, на дне матки и на входе в перешеек фаллопиевых труб наблюдаются обрывки эндометрия.
МРТ (магнитно-резонансное исследование) помогает благодаря контрасту тканей провести наглядную визуализацию патологии. Показанием для проведения МРТ служит:
- Лейомиома матки с подозрением на гиперплазию эндометрия, требующие хирургического лечения.
- Киста яичника и сопутствующие ей заболевания — гиперплазия эндометрия и эндометриоз.
- Диагностика заболеваний матки при синдроме поликистоза яичников.
- Подозрение на рак эндометрия.
- Маточное кровотечение в предклимактерический период.
Лабораторные анализы крови на гормоны помогают выявить дисбаланс гормонов.
5
Типы гиперплазии эндометрия
Гиперплазия отличается развитием осложнений, разные типы гиперплазии подразумевают различную стратегию лечения. Гиперплазия бывает железистой, железисто-кистозной и атипической. Очень редко диагностируется базальная форма гиперплазии. Наиболее легкой формой заболевания считается железистая гиперплазия, которая также делится на острую и хроническую форму заболевания. При железистой гиперплазии происходит изменение формы и расположения желез ткани. Отсутствуют атипичные клетки, не увеличивается количество клеток стромы.
Железисто-кистозная форма заболевания характеризуется разрастанием железистой ткани, появлением кист с жидкостью в тканях слизистой оболочки матки. Очень редко перерождается в злокачественное новообразование. Атипичная форма заболевания мало отличается от железистой формы заболевания, кроме одного – в тканях обнаруживаются атипичные клетки. Это признак перерождения эндометрия в опухоль. Аденоматоз (атипичная гиперплазия) поражает не только железистый слой эндометрия, а также затрагивает базальный слой. Эта форма заболевания склонна к рецидивам, без проведения адекватного лечения переходит в стадию опухолевого процесса.
Гиперплазия может быть очаговой или диффузной. Очаговая форма – это частичное поражение эндометрия заболеванием. При такой форме заболевания возможно наступление беременности. Диффузная форма заболевания – это равномерное поражение эндометрия, при этой форме патологии шанс на беременность минимальный, возрастает риск прерывания беременности на ранних сроках. Гиперплазия и сопутствующая ей миома осложняют течение друг друга, сопровождаются кровотечениями, анемией, наиболее частое осложнение при совокупности заболеваний – это стойкое бесплодие.
Миома матки встречается очень часто, заболевание поражает женщин в любом возрасте. Чаще всего миомы диагностируют в предклимактерическом периоде, когда идет гормональная перестройка организма. Миома похожа на эндометрий повышенным содержанием рецепторов к половым гормонам. Миома матки так же чутко реагирует на гормональные изменения, как эндометрий. И гиперплазия эндометрия, и миома являются гормонозависимыми заболеваниями. При гиперплазии нарушается чувствительность рецепторов эндометрия к гормонам, изменяется местный иммунитет. В отличие от миомы, растущей в мышечном слое органа, гиперплазия эндометрия склонна к перерождению в злокачественное заболевание. Миома никогда не перерождается в злокачественную опухоль.
Миома матки имеет несколько разновидностей: субсерозная, субмукозная, интерстициальная. Миомы бывают множественные и одиночные, смешанные виды. Субсерозная миома расположена на наружной стороне матки, растет в сторону брюшной полости, особую опасность представляет субсерозная миома на ножке. Перекрут ножки, что случается с такими миомами довольно часто, приводит к прекращению питания опухоли и ее некрозу. Растущая субсерозная миома может сдавливать органы брюшной полости, вызывать нарушение кровообращения в органах и тканях, воспалительные процессы.
Субмукозная миома находится под слизистым слоем матки, растет в сторону полости матки. Растущая миома сужает полость детородного органа, часто становится причиной невынашивания беременности. Субмукозная миома на ножке может выпадать в шейку матки, влагалище. Интерстициальная (интрамуральная) миома находится внутри мышечной стенки детородного органа. Также может развиваться межсвязочная миома (интралигаментарная) и миома шейки матки.
7
Лечение гиперплазии эндометрия
Так как общим фактором развития миомы матки и гиперплазии эндометрия является нарушение соотношения гормонов и нарушение работы эндокринной системы, лечение заболеваний состоит из сочетания консервативного (гормональной терапии), хирургического, и в некоторых случаях радикального метода лечения. Радикальный метод лечения применяется в крайнем случае, когда другие методы не принесли успеха. Удаление матки часто сопровождается различными осложнениями, которые могут возникнуть как во время операции, так и после нее.
За последние годы были разработаны неинвазивные методы лечения миомы матки в совокупности с гиперплазией эндометрия, органосохраняющие методики, комплексные методы лечения – органосохраняющий метод + гормональная терапия. Медикаментозное лечение гиперплазии включает использование агонистов и антагонистов ГнРГ. Некоторым больным назначают абляцию эндометрия (при обильных и длительных менструациях), в тяжелых случаях гистерэктомию, овариэктомию. Лечение типичной железистой формы гиперплазии женщинам в детородном возрасте проводят с помощью прогестагена, прогестерона, КОК.
Лечение миомы проводится несколькими органосохраняющими методами. К ним относятся: гистероскопическая миомэктомия, лапароскопическая миомэктомия, ФУЗ-аблация, эмболизация маточных артерий (ЭМА). Лечение с помощью ЭМА имеет большое количество преимуществ, но не всегда проводится, если есть гиперплазия эндометрия. Лечение миомы матки с помощью ЭМА при гиперплазии эндометрия имеет свои показания и противопоказания. Противопоказанием к проведению ЭМА служат следующие патологические состояния: острые воспалительные заболевания органов малого таза, саркома матки, опухоли и кисты яичника, аденокарцинома, атипическая гиперплазия эндометрия. К общим противопоказаниям относится аллергия на контрастное вещество, которое вводится при проведении ЭМА, почечно-печеночная недостаточность. Перед выполнением ЭМА проводят лечение гиперплазии эндометрия, что позволяет достичь большей эффективности в лечении миомы матки. Лечение эндометрия проводится с помощью гормональной терапии, выскабливания функционального слоя, гистероскопической резекции эндометрия.
Эмболизация маточных артерий не требует проведения общего наркоза, процедура проходит быстро и безболезненно. Эндоваскулярный хирург делает прокол в области бедренной артерии, вводит катетер с эмболами и красящим веществом. Под контролем рентген оборудования (изображение процедуры выводится на экран телевизора) хирург подводит катетер к кровеносной системе матки и выпускает эмболы. Эмболы скапливаются в кровеносной системе миомы, сосуды которой являются концевыми и не соединяются с сосудами миометрия, закупоривают сосуды, прекращая снабжение узла кровью. С этого момента начинается процесс деградации миом. Обрабатывается место прокола и накладывается специальный пластырь. На второй день после процедуры пациентка отправляется домой.
Эффективность лечения гиперплазии эндометрия и миомы зависит от своевременности обращения, размера миомы, ее вида, вида гиперплазии, состояния здоровья женщины. Из всех видов гиперплазии наиболее легко поддается лечению железистая гиперплазия. Своевременная диагностика и несколько месяцев лечения под присмотром врача приводят к полному выздоровлению. Более сложным становится лечение железисто-кистозной формы заболевания, тяжелая атипичная форма заболевания чаще всего лечится радикальным методом – удалением матки. Миома матки хорошо поддается лечению при небольших размерах образования, с помощью ЭМА можно удалять миомы различного размера. Эмболизация артерий позволила добиться успеха в лечении множественных миом за одну процедуру. Чтобы получить адекватное и эффективное лечение, избежать врачебной ошибки, следует ответственно отнестись к выбору клиники лечения миомы и врача.
Список литературы
- Савицкий Г. А., Иванова Р. Д., Свечникова Ф. А. Роль локальной гипергормонемии в патогенезе темпа прироста массы опухолевых узлов при миоме матки //Акушерство и гинекология. – 1983. – Т. 4. – С. 13-16.
- Сидорова И.С. Миома матки (современные аспекты этиологии, патогенеза, классификации и профилактики). В кн.: Миома матки. Под ред. И.С. Сидоровой. М: МИА 2003; 5—66.
- Мериакри А.В. Эпидемиология и патогенез миомы матки. Сиб мед журн 1998; 2: 8—13.
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 ноября 2017;
проверки требуют 13 правок.
Миома матки (также фибромиома, лейомиома) — это доброкачественная опухоль, возникающая в мышечном слое матки — миометрии. Является одним из самых распространенных заболеваний у женщин, достигая частоты 12 — 25% от всех гинекологических заболеваний[1]. Наиболее высокая заболеваемость миомой матки приходится на поздний репродуктивный период и перед климаксом[2]. Существует мнение, что истинная распространенность миомы значительно больше и достигает более 70% как в России, так и за рубежом[1][3].
Узел миомы представляет собой клубок хаотично переплетающихся гладкомышечных волокон округлой формы. Большинство узлов имеют диаметр от нескольких миллиметров до нескольких сантиметров, но иногда они могут достигать больших размеров и веса в несколько килограммов. Так, самый большой узел, о котором имеется упоминание в мировой литературе, весил 63 кг[источник не указан 2025 дней].
Причины появления миомы до конца не изучены. Хотя очевидная роль гормональных факторов в развитии миомы была описана еще в 80-е годы прошлого века в трудах В.М. Бреслера и Г.А. Савицкого[4][5][6], остается неясным вопрос первичности или вторичности миомы по отношению к гормональным сдвигам[7]. Существенную роль играют такие факторы риска, как позднее начало месячных, обильные менструации, медаборты, воспалительные заболевания женских половых органов [1][8]. Другим значимым фактором риска считают избыточную массу тела в сочетании с гиподинамией и стрессами [1][9].
Для лечения миомы матки на протяжении многих десятилетий применяется хирургическое удаление узлов (вылущивание) и даже, во многих случаях крупных узлов, — удаление матки. В настоящее время разработаны эффективные схемы консервативного лечения на основе агонистов ГнРГ, а также эффективные эндоваскулярные методики безоперационного лечения миомы с помощью введения в артерии миомы микроэмболов, перекрывающих кровоток в опухоли[10]. Данные методики позволяют сохранить матку в тех случаях, когда раньше была показана гистерэктомия[11].
Механизм развития[править | править код]
Каждый узел миомы возникает в результате неправильного деления одной гладкомышечной клетки, и поэтому все клетки в узле являются идентичными. Миома матки считается гормонально-зависимой опухолью. Доказательством этого служат следующие факторы:
- обнаружение в опухоли рецепторов к половым гормонам,
- появление миомы в репродуктивном возрасте, когда уровень эстрогенов высокий,
- регресс опухоли после менопаузы, когда уровень эстрогенов достигает минимума,
- появление миомы у некоторых женщин в постменопаузе на фоне приема эстрогенных препаратов.
- механизм гиперэстрогении:
- лейомиомы преобразуют эстрадиол в эстрон;
- клетки лейомиомы содержат большую плотность рецепторов (гормонзависимая опухоль) по сравнению с нормальным миометрием;
- лейомиомы содержат высокие уровни цитохром p450 ароматазы, который позволяет преобразовывать андрогены в эстрогены.
Распространенность[править | править код]
Миома матки — самая распространенная опухоль у женщин. По различным оценкам, она возникает у каждой второй-четвертой женщины в течение репродуктивного периода, преимущественно после 30 лет
.
Классификация[править | править код]
По количеству узлов:
- одиночная миома;
- множественная миома.
По расположению узлов в матке:
- Подслизистые узлы (субмукозная миома) — расположены ближе к полости матки. Встречаются относительно редко, иногда они имеют тонкую ножку и могут опускаться из матки в шейку матки или во влагалище; в этом случае говорят о «рождающемся» узле миомы.
- Межмышечные узлы (интерстициальную, интрамуральную) — узлы находятся в стенке матки в мышечном слое.
- Подбрюшинные узлы (субсерозная миома) — расположены на наружной стороне матки, ближе к брюшной полости. Могут иметь основание меньшего диаметра, чем сам узел; в этом случае употребляют термин «узел на ножке».
- Межсвязочные узлы (интралигаментарная миома).
- Шеечная миома.
Наиболее распространенной является интерстициальная миома матки. По данным разных авторов её частота колеблется от 50 до 61% и более. Частота субсерозной миомы от 26 до 35%, субмукозной не более 13% [12].
В 50% случаев миома матки протекает бессимптомно[13]. Бессимптомное течение более характерно для небольшой одиночной или множественной миомы с межмышечным и подбрюшинным расположением[источник не указан 2017 дней].
Симптомы[править | править код]
Наиболее типичными симптомами миомы матки являются сильные менструальные кровотечения (меноррагии), чувство давления и боли внизу живота. Меноррагии более характерны для подслизистых миом. При росте миомы менструации постепенно становятся более обильными и продолжительными, нередко приводя к развитию малокровия (анемии). Чувство тяжести или давления внизу живота более характерно для межмышечной и подбрюшинной миомы, особенно при больших размерах узлов. Боли, как правило, возникают во время менструаций и носят схваткообразный характер, но могут быть постоянными. Боли также могут иметь внезапный режущий характер, что отмечается при очень редком осложнении — перекруте ножки подбрюшинного узла. К более редким симптомам миомы матки относят бесплодие и нарушение функции соседних органов: мочевого пузыря и прямой кишки.
Диагностика[править | править код]
Для диагностики миомы матки наиболее информативным методом является ультразвуковое исследование, при котором миома обнаруживается в виде округлых очагов пониженной эхогенности (имеющих менее плотную структуру, чем миометрий). В некоторых случаях для дифференциальной диагностики миомы матки и опухоли яичника используют магнитно-резонансную томографию.
Основные методы диагностики миомы матки:
- гинекологический осмотр;
- стандартные гинекологические анализы на микрофлору, цитологию, инфекции;
- анализ крови на гормоны;
- трансвагинальное или трансабдоминальное УЗИ;
- магнитно-резонансная томография (МРТ);
- биопсия.
Лечение[править | править код]
Тактика лечения миомы в значительной мере определяется размерами и количеством узлов, а также степенью выраженности симптомов. При бессимптомных миомах малых размеров часто применяется выжидательная тактика, хотя её оправданность остается спорной [14]. Каким бы малым ни был размер узлов миомы — это точно такое же заболевание, и даже крошечные миоматозные узлы, случайно выявленные во время ультразвукового исследования, должны рассматриваться в качестве терапевтической мишени[15].
Консервативная терапия[править | править код]
Из лекарственных препаратов, использующихся при лечении миомы матки и её симптомов, находят применение следующие:
- Транексамовая кислота. Наиболее эффективное средство при меноррагиях, обусловленных миомой матки. Препарат препятствует разрушению тромбов, блокируя эндометриальный плазминоген. Клинические исследования показывают уменьшение менструальной кровопотери на одну треть.
- Антагонисты гонадотропин релизинг-гормона (ГнРГ). Подавляя выработку гонадотропных гормонов гипофиза, оказывают выраженный антиэстрогенный эффект и вызывают значительное уменьшение размеров узлов миомы. Поскольку эффект агонистов ГнРГ наблюдается только во время использования препаратов, а сроки их применения ограничены побочными эффектами, их используют в основном для подготовки к хирургическому удалению узлов.
Широко назначавшиеся ранее оральные контрацептивы и синтетические прогестагены в клинических исследованиях не обнаружили преимуществ в сравнении с плацебо для торможения роста миомы матки. Так, например, препарат Дюфастон®, часто назначаемый при миоме матки, не только не замедляет, но по некоторым данным ускоряет рост узлов[16].
Хирургическое лечение[править | править код]
До недавнего времени гистерэктомия была единственным методом лечения симптомной миомы. В настоящее время гистерэктомия применяется все реже, уступая место более современным, малотравматичным и высокоэффективным методам[10]. Из эндоскопических методов для удаления подбрюшинных узлов миомы используются лапароскопия, а для удаления подслизистых узлов — гистероскопия.
Эмболизация маточных артерий[править | править код]
Современный метод лечения миомы матки, принцип которого состоит в прекращении кровотока по маточным артериям, и замещении узлов миомы соединительной тканью[17]. Метод заключается в проведении катетера через бедренную артерию в маточную артерию и блокировании в ней кровотока с помощью эмболизационного материала. Процедура выполняется в рентгеноперационной, относится к малоинвазивным вмешательствам и не требует наркоза. Как правило, необходима госпитализация на один день. В настоящее время эмболизация все шире применяется для лечения миомы матки.
ФУЗ-абляция миомы[править | править код]
Метод лечения миомы, основанный на нагревании тканей узлов высокоинтенсивым фокусированным ультразвуком, благодаря передаче большого количества энергии в четко локализованный участок после применения которого наступает деструкция ткани узла — термический некроз. Принцип действия очень напоминает концентрацию солнечных лучей увеличительным стеклом. Вершиной развития метода является на сегодняшний день комбинация источника фокусированного ультразвука (излучатель вмонтированный в стол) и аппарата МРТ. Проведение ультразвука осуществляется через переднюю брюшную стенку. МР томограф контролирует локализацию и что особенно важно температуру нагрева в режиме реального времени. Метод позволяет проводить деструкцию четко ограниченного участка, не повреждая здоровые ткани. Зона между «пролеченной» и здоровой тканью составляет всего лишь несколько рядов клеток. Таким образом фокусированный ультразвук на сегодняшний день как никогда близко приблизился к понятию «идеальный хирургический инструмент» Процедура не требует введения инструментов в полости тела, обезболивания и госпитализации, однако возможна далеко не во всех случаях и требует правильного отбора пациентов. Субстратом для воздействия фокусированного ультразвука является соединительная ткань расположенная в миоме. Соединительная ткань хорошо накапливает энергию и позволяет достичь температуру необходимую для термического некроза. Таким образом очень хорошо лечению методом ФУЗ поддаются так называемые фибромиомы, которые составляют 70% всех миом. Лейомиомы, или клеточные миомы абсолютно не подходят к лечению методом ФУЗ из-за отсутствия субстрата для воздействия и высокоинтенсивному кровоснабжению, что не позволяет провести достаточный нагрев ткани. В период тестирования метода и его внедрения в клиническую практику неправильный отбор пациенток служил причиной частых рецидивов и ошибочно трактовался как неэффективность метода. Для оценки возможности проведения ФУЗ абляции пациентки необходимо пройти МРТ при которой определяется тип миомы. В последнее время многочисленными работами различных авторов [18], основанными на ретроспективных исследованиях пролеченных пациенток, показана высокая эффективность метода, не уступающая по показателям другим методам лечения миомы матки при условии его правильного применения[19][20][21].
Показаниями к применению ФУЗ-абляции в отношении миомы матки являются стандартные показания к органосберегающему лечению при миоме матки. В зависимости от клинических задач, которые ставит врач-гинеколог, применение технологии возможно в четырех тактических вариантах.
1. Органосберегающее лечение миомы матки.
2. Профилактика клинических проявлений миомы матки (что позволяет отказаться от выжидательной амбулаторной практики в отношении роста миоматозных узлов).
3. Подготовка узла миомы к трансцервикальной миомэктомии (в результате FUS-деструкции уменьшаются размеры узла и интенсивность кровотока, что существенно снижает риск возможных осложнений и облегчает проведение операции);
4. С целью отсрочить оперативное лечение.
В отличие от других методов, ФУЗ-МРТ абляция миомы матки — это неинвазивный, органосберегающий метод, без госпитализации, без боли, сохраняет женщине максимально высокие шансы в сравнении с другими методами на успешную беременность, имеет минимальный процент осложнений среди всех используемых методов лечения миомы матки (в настоящее время менее 0,05%).
Метод получил признание во многих странах CE (Европа), FDA (США), MHLW (Japan), CFDA (China), ANVISA (Brazil), Canada FDA, KFDA (Korea), РФ, Тайвань.
Другие виды лечения[править | править код]
Для лечения миомы используются экстракты лекарственных растений и гомеопатические препараты, однако эффективность их не является доказанной.
Профилактика[править | править код]
Специальных мер предупреждения миомы матки не существует.
Примечания[править | править код]
- ↑ 1 2 3 4 Буянова С. Н., Мгелиашвили М. В., Петракова С. А. Современные представления об этиологии, патогенезе и морфогенезе миомы матки //Российский вестник акушера-гинеколога.–2008.–Т. – 2008. – Т. 8. – С. 45-51. (недоступная ссылка)
- ↑ Сидорова И.С. Миома матки (современные аспекты этиологии, патогенеза, классификации и профилактики). В кн.: Миома матки. Под ред. И.С. Сидоровой. М: МИА 2003; 5—66.
- ↑ Мериакри А.В. Эпидемиология и патогенез миомы матки. Сиб мед журн 1998; 2: 8—13.
- ↑ Савицкий Г. А. и др. Локальная гормонемия матки и рецепторы стероидных гормонов //Акушерство и гинекология. – 1985. – №. 2. – С. 19-22.
- ↑ Вихляева Е. М., Савицкий Г. А. Миома матки. Патогенетические и терапевтические аспекты //Акуш. и гин. – 1996. – №. 6. – С. 56.
- ↑ Савицкий Г. А., Иванова Р. Д., Свечникова Ф. А. Роль локальной гипергормонемии в патогенезе темпа прироста массы опухолевых узлов при миоме матки //Акушерство и гинекология. – 1983. – Т. 4. – С. 13-16.
- ↑ Ланчинский В.И., Ищенко А.И. Современные представления об этиологии и патогенезе миомы матки. Вопр гин акуш и перинат 2003; 2: 5—6: 64—69.
- ↑ Вихляева Е.М. Руководство по диагностике и лечению лейомиомы матки. М: МЕДпресс-информ 2004; 400.
- ↑ Рыжова О.О. Патогенетические аспекты роста миоматозных узлов. В кн.: Миома матки. Под ред. И.С. Сидоровой. М: МИА 2002: 98—112.
- ↑ 1 2 Капранов С. А. и др. Новый органосохраняющий метод лечения миомы матки-эмболизация маточных артерий //Лечебное дело. – 2005. – №. 2.
- ↑ Лубнин Д. М., Тихомиров А. Л. Селективная эмболизация маточных артерий в алгоритме органосохраняющего лечения миомы матки : дис. – Москва : [Моск. гос. медико-стоматол. ун-т МЗ РФ], 2005.
- ↑ Медведев М. В., Лютая Е. Д. Миома матки //Допплерография в гинекологии: Энциклопедия ультразвуковой диагностики в акушерстве и гинекологии./Под ред. Зыкина БИ, Медведева МВМ; Реальное время. – 2000. – С. 45-58. (недоступная ссылка)
- ↑ Srividhya Sankaran, Isaac T. Manyonda. Medical management of fibroids. Best Practice & Research Clinical Obstetrics and Gynaecology Vol. 22, No. 4, pp. 655–676, 2008 doi:10.1016/j.bpobgyn.2008.03.001
- ↑ Петракова С. А., Буянова С. Н., Мгелиашвили М. В. Возможности миомэктомии в коррекции репродуктивного здоровья женщин с миомой матки //Российский вестник акушера гинеколога. – 2009. – №. 1. – С. 30-34. (недоступная ссылка). Дата обращения 16 июля 2014. Архивировано 25 июля 2014 года.
- ↑ Андроутопулос Г., Декавалас Г. Последние достижения в лечении миомы матки (недоступная ссылка). Перевод с англ. Н. Д. Фирсовой (2018).
- ↑ Тихомиров А. Д., Лубнин Д. М. Миома матки. Архивная копия от 24 мая 2018 на Wayback Machine 2006, ISBN 5-89481-417-0
- ↑ Б. Ю. Бобров, С. А. Капранов, В. Г. Бреусенко и др. Эмболизация маточных артерий: современный взгляд на проблему. «Диагностическая и интервенционная радиология» том 1 № 2 / 2007
- ↑ Incidence of Additional Treatments in Women Treated with MR-Guided Focused US for Symptomatic Uterine Fibroids: Review of 138 Patients with an Average Follow-up of 2.8 Years Krzysztof R. Gorny, PhD, Bijan J. Borah, PhD, Douglas L. Brown, MD, David A. Woodrum, MD, PhD, Elizabeth A. Stewart, MD, and Gina K. Hesley, MD
- ↑ Gorny KR, Woodrum DA, Brown DL, et al. Magnetic resonance-guided focused ultrasound of uterine leiomyomas: review of a 12-month outcome of 130 clinical patients. J Vasc Interv Radiol 2011; 22:857–864
- ↑ Park Min J, Kim Y, Rhim H, et al. Safety and therapeutic efficacy of complete or near-complete ablation of symptomatic uterine fibroid tumors by MR imaging-guided high intensity focused US therapy. J Vasc Interv Radiol 2014; 25:231–239
- ↑ Лечение больных с миомой матки фокусированным ультразвуком под контролем магнитно-резонанской томографии: клиническая безопасность, возможные осложнения Курашвили Ю.Б, Г.Е Саламандина, Чмыр Е.Н.,О.И. Батаршина., РОССИЙСКИЙ ВЕСТНИК АКУШЕРА-ГИНЕКОЛОГА 2, 2010 стр. 56-60
Ссылки[править | править код]
- Комплексная консервативная терапия миомы матки в сочетании с аденомиозом: применение препарата «Курантил» Consilium medicum
- Патология эндометрия при наличии миомы матки Consilium medicum
- Неоперативные методы лечения миомы матки Медицинский журнал Лечащий врач